1、Trilaciclib改善化疗引起的骨髓抑制
化疗引起的造血干/祖细胞(HSPC)损伤会引起多系的骨髓抑制。Trilaciclib是一种静注使用的CDK4/6抑制剂,可在化疗过程中主动保护HSPC以及增加免疫系统功能。近期发表在《Annals of Oncology》上的一项临床研究显示,Trilaciclib可使HSPC暂时停滞在G1期并使其免受化疗损伤,从而加快造血恢复的时间,改善化疗相关不良反应的发生。
该项Ib期(开放标签、剂量探索)和II期(随机、双盲、安慰剂对照)研究Trilaciclib与依托泊苷/卡铂(EP)联合一线治疗广泛期小细胞肺癌(SCLC)的安全性、有效性和药代动力学研究。研究终点是Trilaciclib对骨髓抑制以及抗肿瘤疗效的影响。
研究共招募了122名患者。使用Trilaciclib后,中性粒细胞、红细胞和淋巴细胞的数量都出现了升高。与EP联合治疗的安全性也得到了改善,与联合安慰剂相比≥3级不良事件发生更少(50% vs 83.8%),而这一获益主要来源于血液毒性的改善。
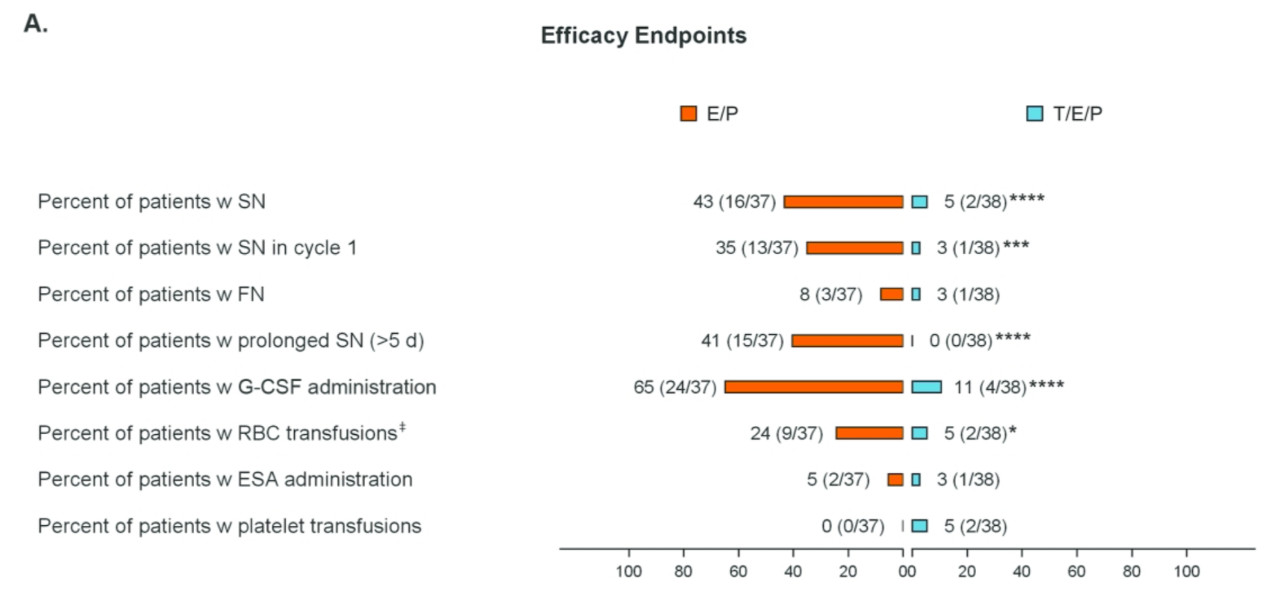
图1 联合Trilaciclib后治疗相关血液学毒性的发生明显降低
在抗肿瘤治疗疗效方面,联合trilaciclib对比联合安慰剂:客观缓解率(ORR:66.7% vs 56.8%, p=0.3831);中位无进展生存期(PFS:6.2m vs 5.0m;HR 0.71;p=0.1695);总生存期(OS:10.9m vs 10.6m;HR 0.87;p=0.6107)均未见明显差异。
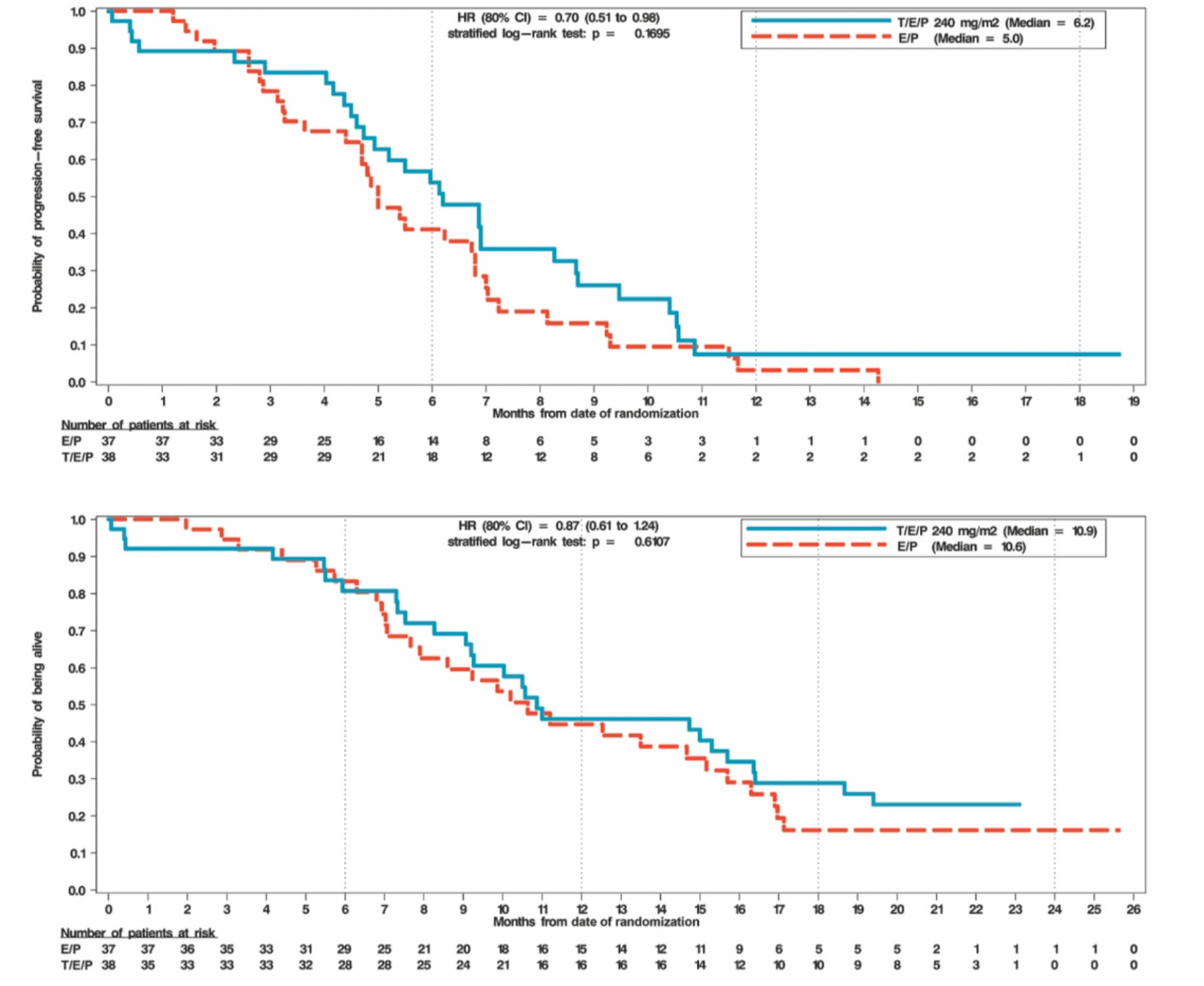
图2 两组生存曲线未见明显差异
该研究证实了Trilaciclib辅助患者改善对化疗的耐受性,保存了患者多系的骨髓造血功能,因此治疗不良反应相关的剂量降低的事件发生也更少,改善了治疗的安全性,同时对治疗抗肿瘤疗效没有降低。
02 复发性SCLC:可尝试K药联合紫杉醇治疗
依托泊苷/铂类耐药的广泛期小细胞肺癌(ED-SCLC)患者预后不良,免疫治疗值得尝试,近期,《Lung Cancer》在线发表的帕博利珠单抗(俗称“K药”)、紫杉醇联合二线治疗的疗效和安全性研究发现,ORR达到23.1%,PFS为5个月,OS为9.1个月,显示出一定的疗效。
在这项多中心II期研究中,依托泊苷/铂类化疗后进展的ED-SCLC患者每3周接受紫杉醇175 mg/m2,最多6个周期。从第二周期加入帕博利珠单抗200mg并持续至疾病进展或不可接受的毒性。研究的主要终点是ORR,次要终点是无进展生存期PFS、OS、安全性和生物标志物分析。
结果显示,在入组的26名患者中,ORR为23.1%(95%CI:6.9%-39.3%),其中完全缓解3.9%,部分缓解19.2%,疾病稳定57.7%,疾病进展7.7%,NA:11.5%。疾病控制率(DCR)达到80.7%。中位PFS和OS分别为5.0个月(95%CI:2.7-6.7)和9.1个月(95%CI:6.5-15.0)。
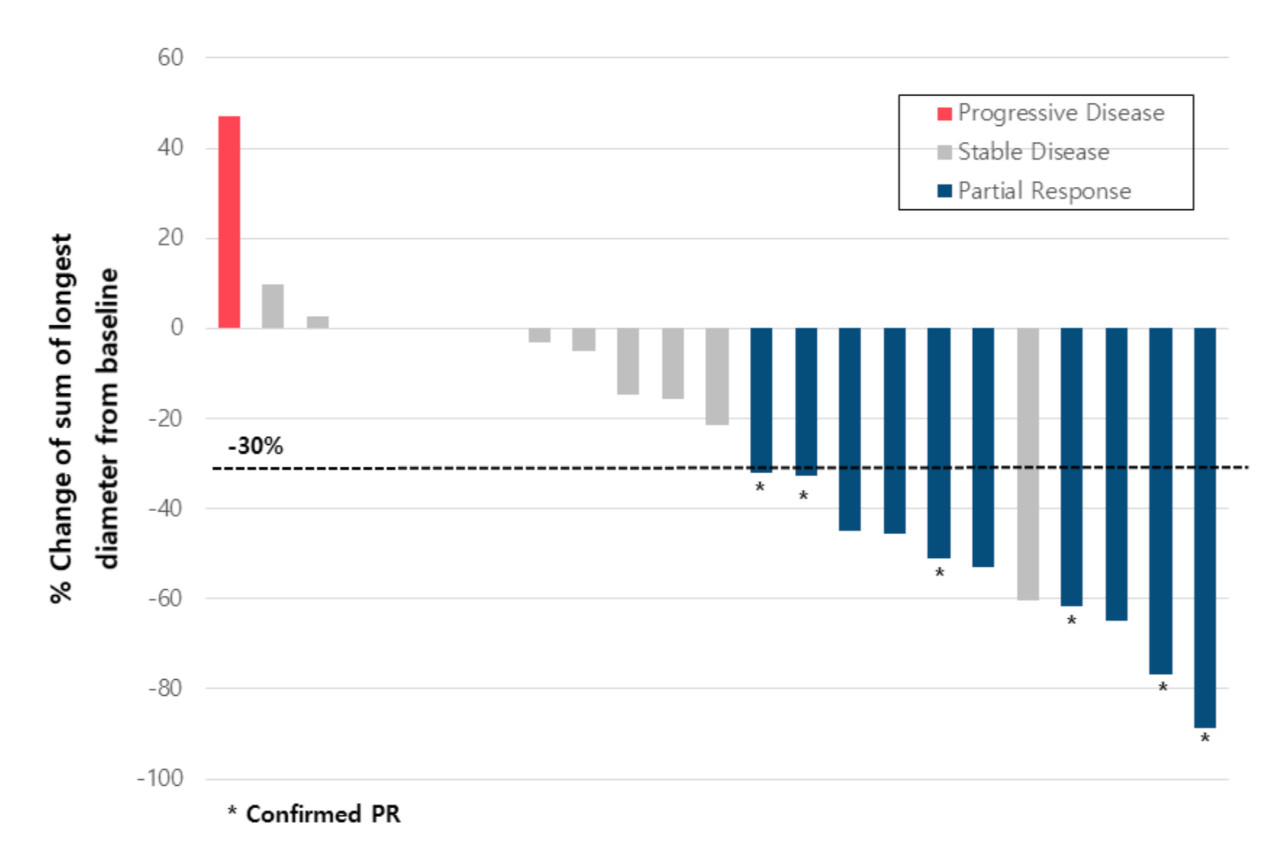
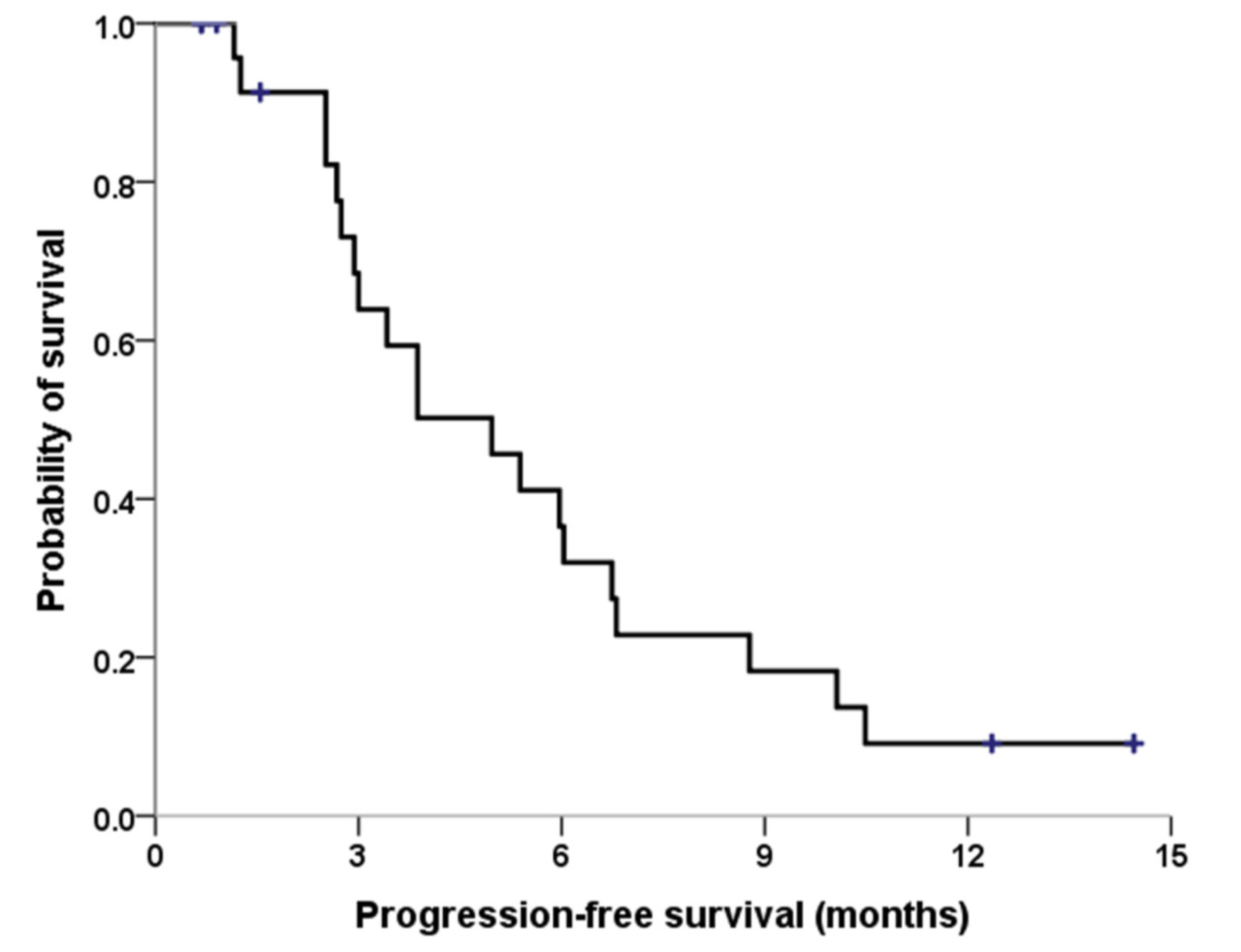
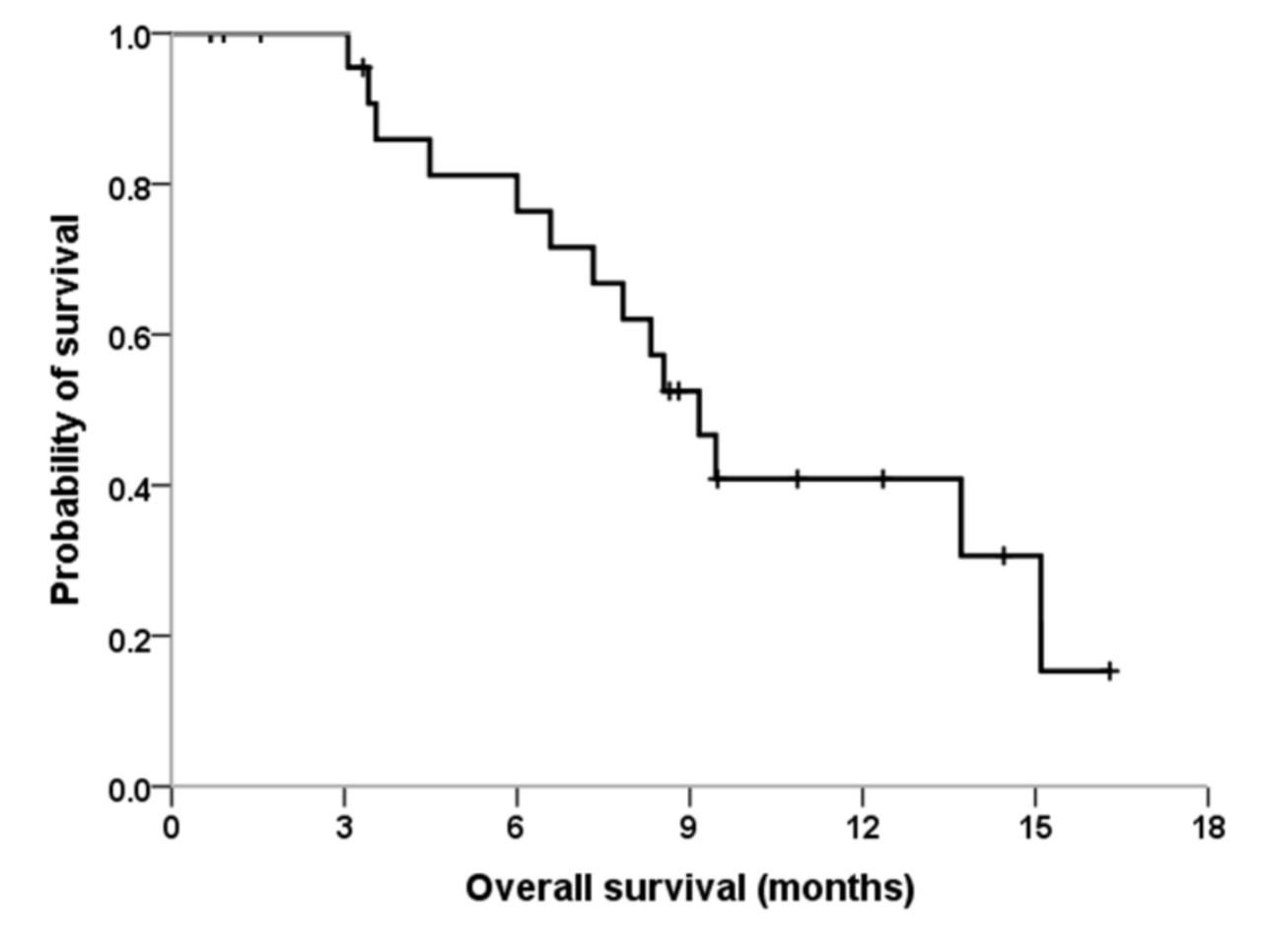
图3 疗效瀑布图
图4 生存分析 3-4级不良事件包括发热性中性粒细胞减少症(7.7%)、中性粒细胞减少症(7.7%)、虚弱乏力(7.7%)、低钠血症(7.7%)和I型糖尿病(7.7%)。研究发现MET拷贝数增加与不良预后相关(PFS:10.5 vs 3.4个月,p=0.019),而靶向基因测序未发现其余与治疗相关的特定遗传改变。表1 不良反应汇总
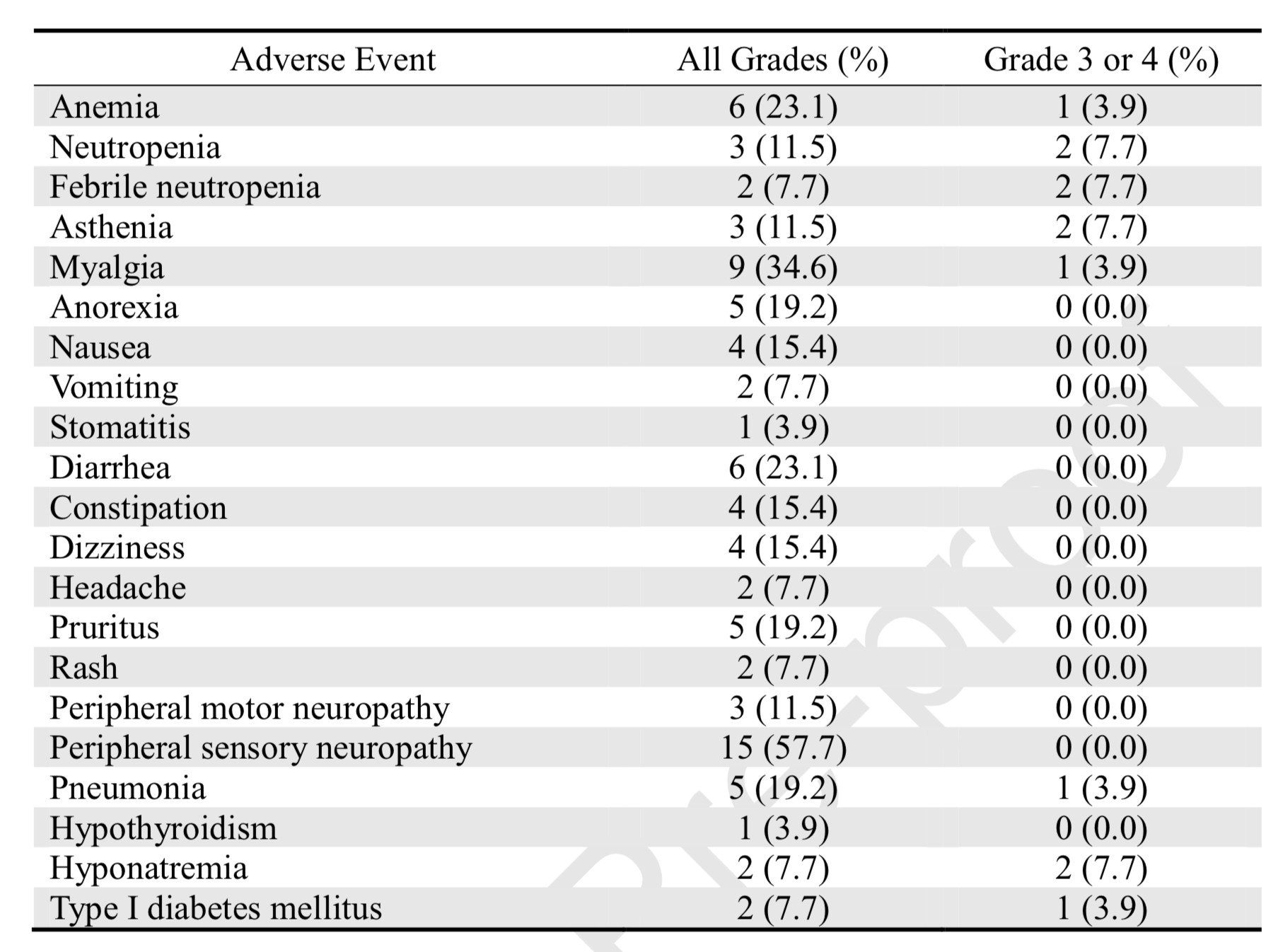
该研究认为,帕博利珠单抗和紫杉醇联合治疗在复发ED-SCLC患者中表现出一定的治疗疗效和可接受的毒性。
03陆舜课题组:液体活检揭示肺腺癌患者肿瘤代谢特征
尽管肺癌的治疗已进入精准治疗的时代,但是在临床实践中仍能观察到具有相同驱动基因改变的患者(EGFR/ALK/ROS1等),接受靶向治疗预后不尽相同。上海胸科医院陆舜教授近日在《Nature Communications》上发表了一篇论著,建立了一种基于液体活检的肿瘤单细胞代谢分型的方法,对肺腺癌患者恶性胸水来源的肿瘤细胞进行单细胞流式芯片代谢和荧光代谢探针分析,解析了肿瘤细胞不同的代谢分型。

图5 研究发表于《Nature Communications》杂志
该研究纳入了32名肺腺癌患者,收集了这些患者的胸腔积液,进行单细胞流式和荧光代谢分析。研究者观察到肿瘤细胞间广泛存在的代谢异质性,可以分成糖酵解(CD45neg /2-NBDGhigh cells)和线粒体氧化(CD45neg C12R high cells)两种代谢表型。两种分型的肿瘤细胞数对患者的治疗疗效和预后具有预测作用。
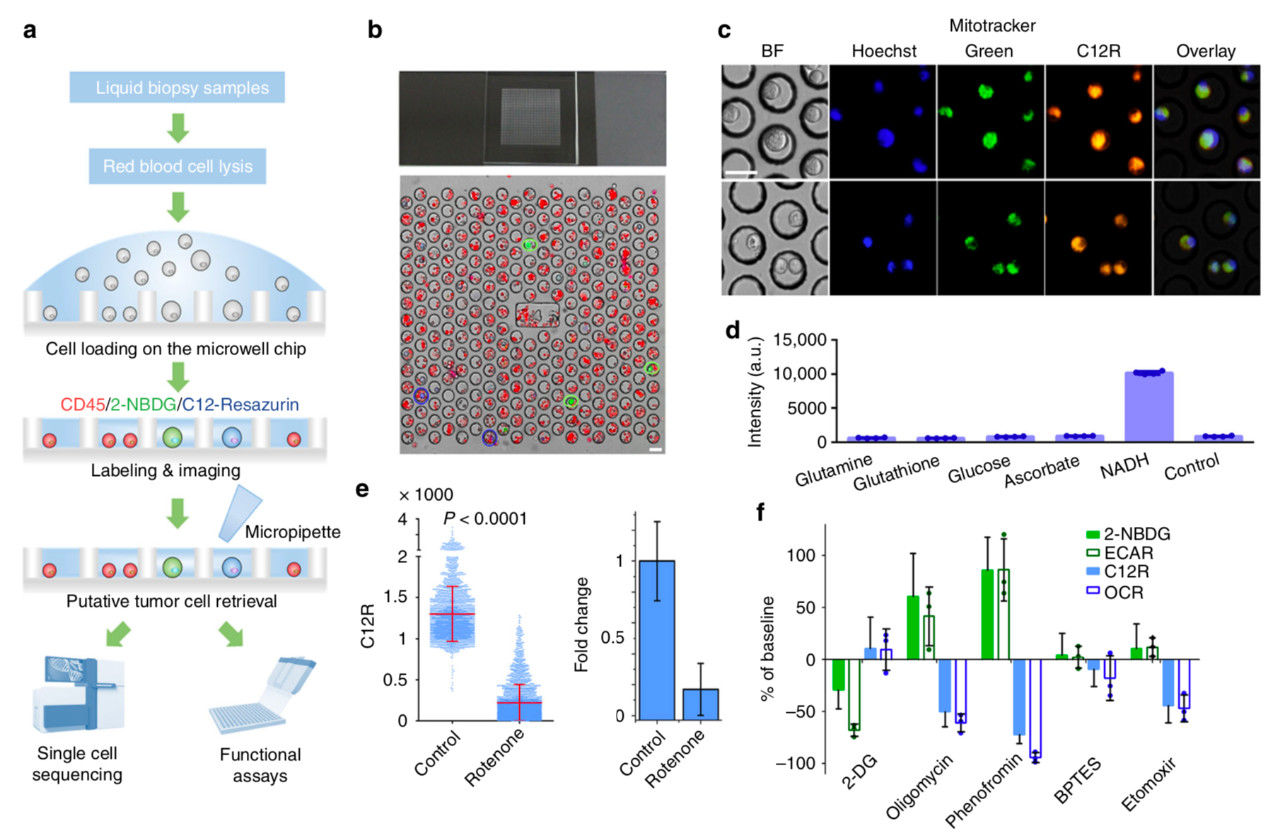
图6 基于液体活检的肿瘤单细胞代谢分型
另外,转录组测序发现,靶向AXL的药物在糖酵解依赖性细胞中能够增加细胞的杀伤功能,但是对线粒体氧化依赖性的细胞没有观察到这一作用。
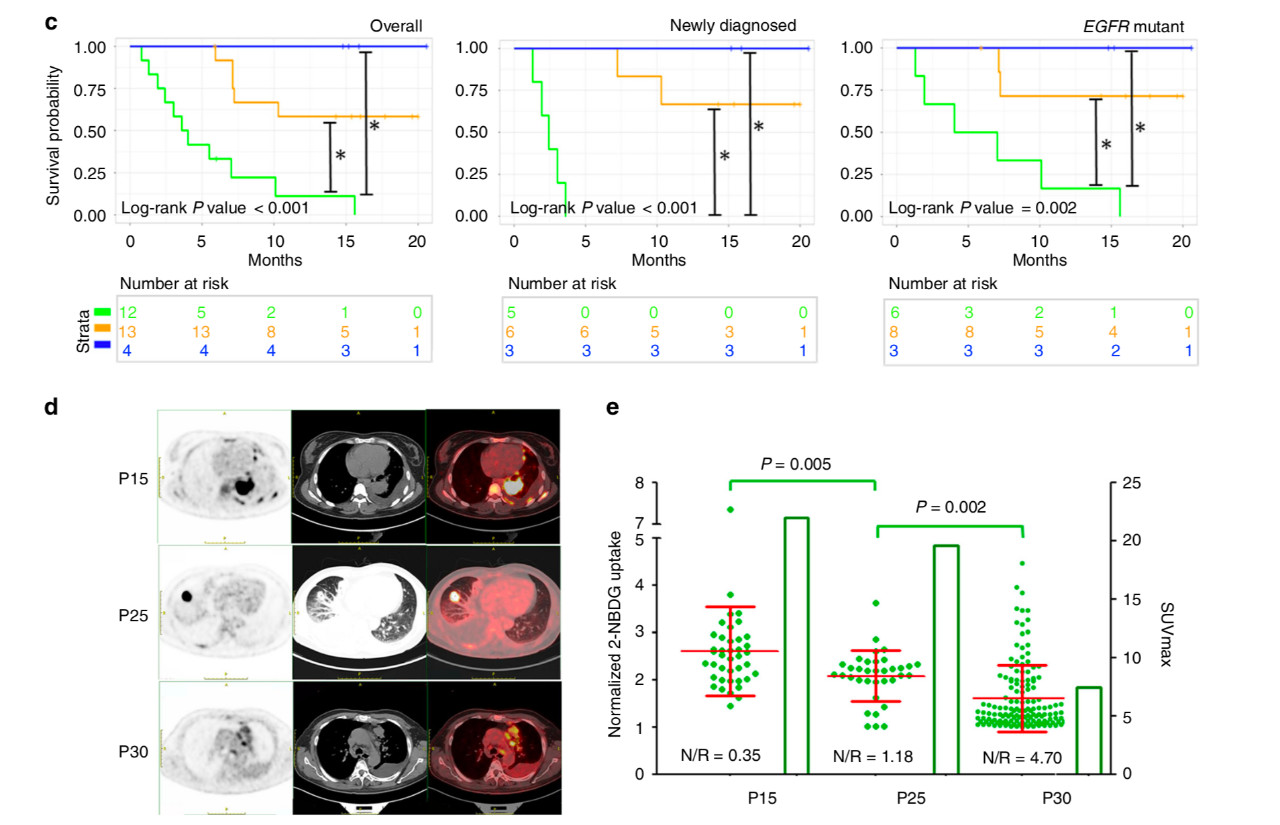
图7 该分型对疗效的预测
该研究解析了具有相同驱动基因的肺腺癌患者具有不同的代谢特征,这一结果对未来进一步精准治疗提供了有力的依据。
参考文献
[1]Weiss J M, Csoszi T, Maglakelidze M, et al. Myelopreservation with the CDK4/6 inhibitor trilaciclib in patients with small cell lung cancer receiving 1st-line chemotherapy: a Phase 1b/randomized Phase 2 trial[J]. Annals of Oncology, 2019.
[2]Kim Y J, Keam B, Ock C Y, et al. A Phase II Study of Pembrolizumab and Paclitaxel in Patients with Relapsed or Refractory Small-Cell Lung Cancer[J]. Lung Cancer, 2019.
[3]Li Z, Wang Z, Tang Y, et al. Liquid biopsy-based single-cell metabolic phenotyping of lung cancer patients for informative diagnostics[J]. Nature communications, 2019, 10(1): 1-16.