一 难治性多发性骨髓瘤:Selinexor方案有效
美国西奈山医院Paul G. Richardson和Sundar Jagannath等开展的STORM研究显示,对于目前标准疗法治疗失败的多发性骨髓瘤患者,选择性核输出抑制剂Selinexor联合地塞米松治疗有效[1-2]。研究结果近日发表于《New England Journal of Medicine》。
■ 研究概要
研究纳入曾接受硼替佐米、卡非佐米、来那度胺、泊马度胺、达雷木单抗和烷化剂治疗,并且对至少一种蛋白酶体抑制剂、一种免疫调节剂和达雷木单抗耐药(triple-class refractory)的骨髓瘤患者,给予口服Selinexor 80 mg联合地塞米松20 mg(每周两次)治疗。主要终点为总缓解,次要终点为临床获益。结果显示,122例患者被纳入改良的意向治疗人群,123例被纳入安全人群。患者的中位年龄为65岁,中位既往治疗方案数为7个,53%患者存在高危细胞遗传学异常。疗效分析显示,26%患者至少获得部分缓解,包括2例严格的完全缓解; 39%患者至少获得最小缓解。中位缓解持续时间为4.4个月(图1),中位无进展生存(PFS)为3.7个月(图2A),中位总生存(OS)为8.6个月(图2B)。
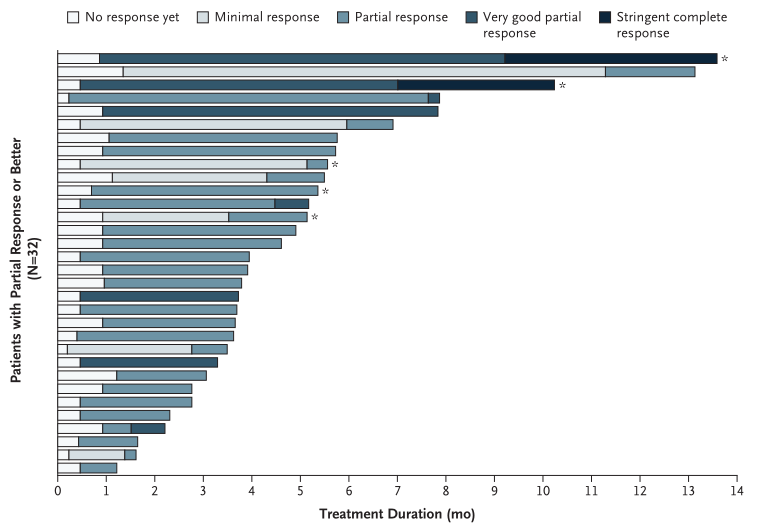
图1 患者的缓解持续时间
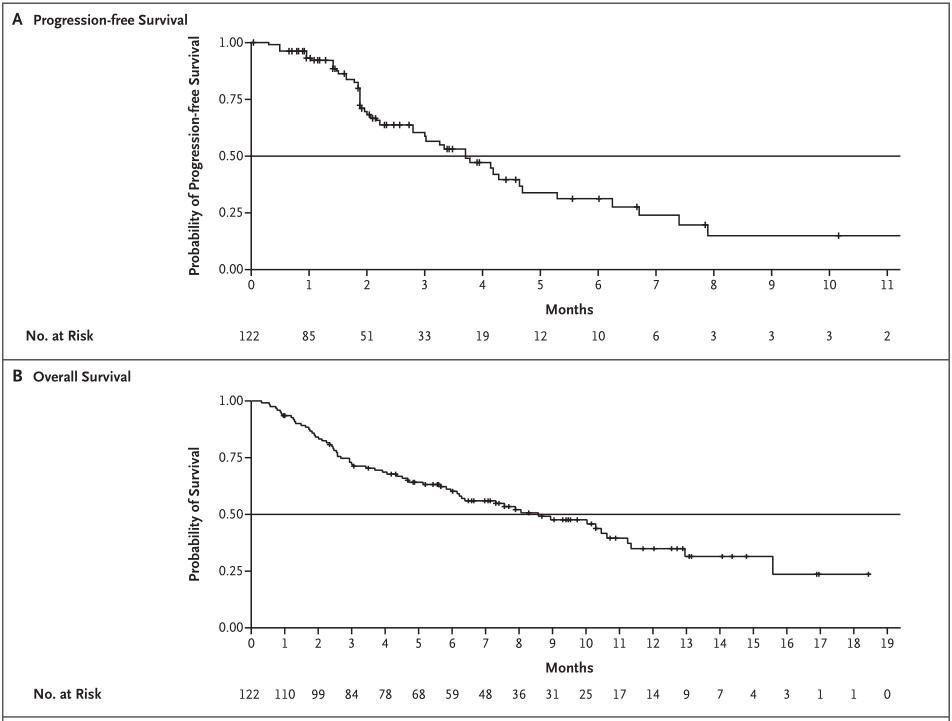
图2 患者的无进展生存和总生存Kaplan–Meier分析基于该研究结果,美国食品药品监督管理局(FDA)已加速批准Selinexor联合地塞米松治疗复发或难治性多发性骨髓瘤。
二 复发/难治性多发性骨髓瘤:双靶点CAR-T治疗初现疗效
徐州医科大学附属医院徐开林教授等的研究显示,对于复发或难治性多发性骨髓瘤患者,人源化抗CD19和抗B细胞成熟抗原(BCMA)嵌合抗原受体T细胞(CAR-T)输注联合方案治疗的总缓解率达95%[3-4]。研究结果发表于《the Lancet Haematology》。 ■ 研究概要该项单中心、单臂、2期临床试验招募了22例复发或难治性多发性骨髓瘤患者,其中21例接受了CAR-T输注且可评估。中位随访179天,21例获得缓解(总缓解率为95%),包括9例(43%)严格的完全缓解,3例(14%)完全缓解,5例(24%)非常好的部分缓解,3例(14%)部分缓解(图3)。
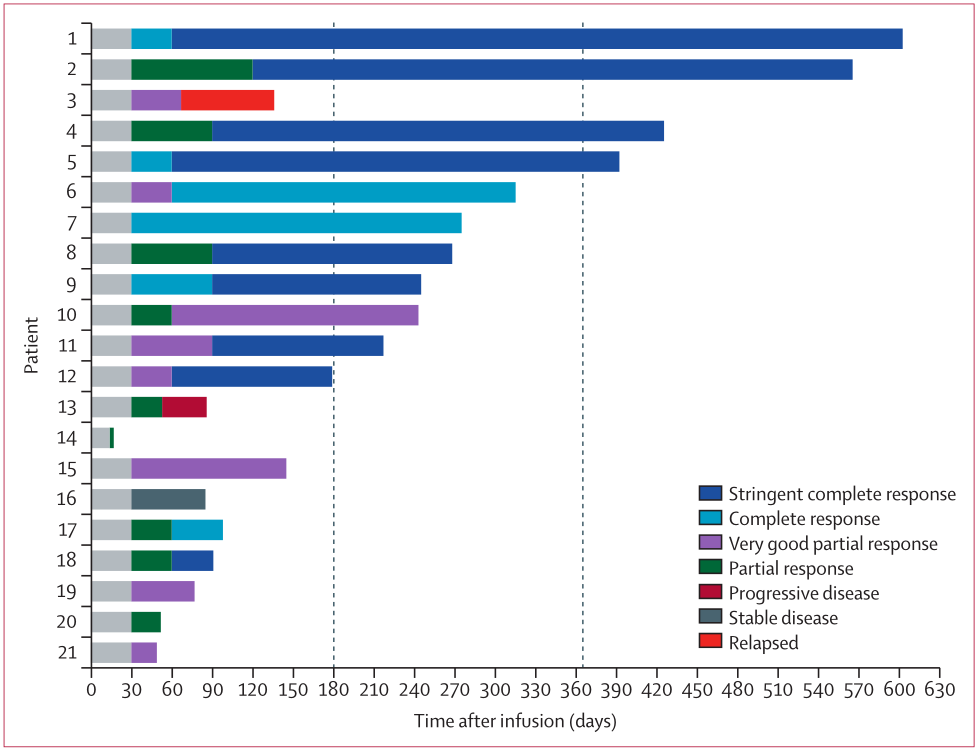
图3 CAR-T输注后的反应评估结果证实,人源化CD19 CAR-T和BCMA CAR-T的联合方案用于复发或难治性多发性骨髓瘤可行,其可能是一种有前景的治疗选择,值得进一步研究。
三 晚期皮肤T细胞淋巴瘤:抗生素可抑制疾病活动
丹麦哥本哈根大学Niels Odum等开展的一项前瞻性研究显示,用于治疗金黄色葡萄球菌的抗生素似乎可抑制晚期皮肤T细胞淋巴瘤(CTCL)患者的疾病活动[5]。研究者指出,抗生素或是CTCL的重要辅助治疗方法。研究结果发表于《Blood》。 ■ 研究概要该研究探讨短暂抗生素治疗对8例晚期CTCL患者肿瘤细胞和疾病活动的影响。研究中,患者接受静脉注射头孢菌素和甲硝唑10天,然后口服阿莫西林和克拉维酸14天。随访2个月后,所有患者表现出临床症状明显改善。2例患者临床症状改善持续超过8个月。6例患者抗生素治疗后恶性T细胞比例显著降低。免疫组织化学、全mRNA表达和细胞信号通路分析显示,短暂、积极的抗生素治疗与受损皮肤中IL-2高亲和力受体(CD25)表达、STAT3信号传导和细胞增殖能力的降低相关。
四 滤泡性淋巴瘤:利妥昔单抗维持治疗带来持久PFS获益
PRIMA研究长期结果显示,在诱导免疫化疗后,滤泡性淋巴瘤患者接受利妥昔单抗维持治疗相比观察等待可获得持久的PFS获益,但两者的OS获益相当[6] 。研究结果发表于《Journal of Clinical Oncology》。研究者表示,该研究为期9年的随访结果表明,诱导免疫化疗后利妥昔单抗维持治疗获得的长期PFS获益显著优于观察等待。尽管缺乏OS优势,但值得注意的是,利妥昔单抗组中超过一半的患者未出现疾病进展,并且超过10年不需要新的抗淋巴瘤治疗。■ 研究概要该项开放标签、多中心、随机、3期研究纳入1,018例初治滤泡性淋巴瘤患者,这些患者接受一线基于利妥昔单抗的免疫化疗诱导方案获得缓解。诱导治疗后,患者被随机分入2年利妥昔单抗维持治疗组(505例)或观察组(513例)。中位随访9年。结果显示,维持治疗组中位PFS显著长于观察组(10.5年 vs 4.1年,HR=0.61),但两组间OS无显著差异(HR=1.04),维持治疗组和观察组估计的10年OS率分别为80.1%和79.9%。
五 骨髓纤维化:Fedratinib获FDA批准
近日,美国FDA批准Fedratinib胶囊用于某些类型骨髓纤维化成人患者的治疗 [7]。Fedratinib是一种高选择性JAK2抑制剂,适用于中危-2或高危原发性或继发性(真性红细胞增多症或原发性血小板增多症后)骨髓纤维化患者。■ JAKARTA研究此次获批是基于关键性3期、多中心、随机、双盲、安慰剂对照试验JAKARTA的研究结果。该研究旨在中危-2或高危原发性骨髓纤维化、红细胞增多症后骨髓纤维化或原发性血小板增多症后骨髓纤维化伴脾肿大的患者中,评估对比Fedratinib(每日口服剂量400 mg或500 mg)与安慰剂的疗效。研究纳入24个国家94个临床中心的289例患者。在96例接受Fedratinib每日剂量400 mg(批准标签中推荐的剂量)治疗患者中,有35例治疗效果显著[在第6治疗周期(24周)结束时,通过MRI或CT扫描评估,脾脏体积比基线时减少≥35%]。此外,36例患者的骨髓纤维化相关症状减少≥50%,包括盗汗、瘙痒、腹部不适等。
六 急性淋巴细胞白血病:超重、肥胖或增加儿童患者的早死风险
墨西哥城UMAE Hospital de Pediatría的研究人员Juan Carlos Núñez-Enríquez等的研究显示,对于患有急性淋巴细胞白血病(ALL)的墨西哥儿童,超重和肥胖是早期死亡的预测因素[8]。研究结果发表于《BMC Cancer》。■ 研究概要该项多中心队列研究纳入1,070例年龄小于15岁的ALL儿童,这些患者在确诊后前24个月内接受了随访。研究者根据世界卫生组织(WHO)和美国疾病控制和预防中心(CDC)标准判定超重和肥胖,并将超重和肥胖作为早期死亡和早期复发的预测因子进行研究。 结果发现,诊断时的超重和肥胖可预测早期死亡(WHO:HR=1.4,95%CI 1.0~2.0;CDC:HR=1.6,95%CI 1.1~2.3)。然而,超重(WHO:HR=1.5,95%CI 0.9~2.5;CDC:HR=1.0,95%CI 0.6~1.6)和肥胖(WHO:HR=1.5,95%CI 0.7~3.2;CDC:HR=1.4,95%CI 0.9~2.3)与早期复发无关联。
参考资料
[1]https://www.healio.com/hematology-oncology/myeloma/news/online/%7Bb6788042-6caa-4081-8b17-8211a56e92f2%7D/selinexor-regimen-induces-response-in-refractory-multiple-myeloma
[2]Chari A, Vogl DT, Gavriatopoulou M, et al. Oral Selinexor-Dexamethasone for Triple-Class Refractory Multiple Myeloma[J]. N Engl J Med. 2019 Aug 22;381(8):727-738.
[3]https://www.healio.com/hematology-oncology/myeloma/news/online/%7B96ccc5c0-0b94-4f1f-ab5a-781f96b15b87%7D/dual-car-t-cell-combination-a-promising-treatment-option-for-multiple-myeloma
[4] Yan Z, Cao J, Cheng H, et al. A combination of humanised anti-CD19 and anti-BCMA CAR T cells in patients with relapsed or refractory multiple myeloma: a single-arm, phase 2 trial[J]. Lancet Haematol. 2019 Aug 1 [Epub ahead of print]
[5]https://www.healio.com/hematology-oncology/lymphoma/news/online/%7Bb94e19d5-ebee-4d52-a791-81b65b3897b6%7D/antibiotics-thwart-disease-activity-in-advanced-cutaneous-t-cell-lymphoma
[6]https://www.healio.com/hematology-oncology/lymphoma/news/online/%7B81a9c132-3ff1-4cd0-a81a-482ec66361d9%7D/rituximab-maintenance-confers-lasting-pfs-benefit-for-patients-with-follicular-lymphoma
[7]https://www.medscape.com/viewarticle/916928
[8]https://medicalxpress.com/news/2019-08-overweight-obesity-early-mortality-pediatric.html