结直肠癌为什么需要基因检测
PART1 结直肠癌概述
01.定义
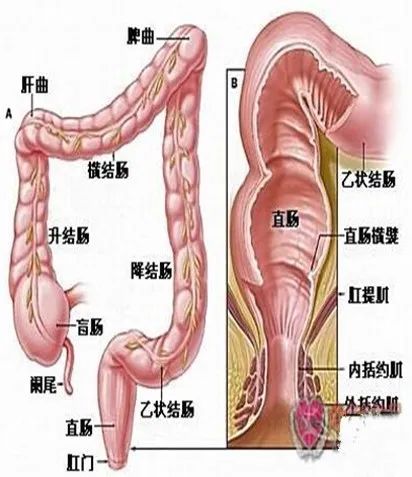
结直肠癌是胃肠道中常见的恶性肿瘤,可以发生在结肠或直肠的任何部位,但以直肠、乙状结肠最为多见,其余依次见于盲肠、升结肠、降结肠及横结肠。
结肠癌是指回盲部至乙状结肠直肠交界处的癌。以横结肠的脾曲为界,将结肠分为左、右半结肠。据统计,2/3的结直肠癌发生于左半结肠,另外1/3则发生于右半结肠。
直肠癌是乙状结肠直肠交界处至齿状线之间的癌。
02.发病机制
发病相关的因素主要包括:饮食因素、疾病因素、家族遗传因素及年龄等。
1. 饮食因素:高脂肪、高蛋白、低膳食纤维素的摄入;维生素缺乏;肠道菌群失调;亚硝酸盐类化合物的摄入
2. 疾病因素:溃疡性结肠炎、大肠息肉和腺瘤等疾病均与CRC有关,目前认为腺瘤性息肉、绒毛状腺瘤、家族性多发息肉病等是CRC的癌前病变
3. 家族遗传因素:遗传相关的结直肠癌的发病率约占CRC的20%,主要包括Lnych综合症、家族性腺瘤息肉病、幼年性息肉病综合征、锯齿形息肉病综合征、色素沉着息肉综合征、李-弗美尼综合征和Cowden综合征、 MUTYH相关性息肉病
4. 年龄因素:既往认为CRC的发病率随着年龄的增大而增高
03.临床表现
早期结直肠癌可无明显症状,病情发展到一定程度可出现下列症状:
—排便习惯改变
—大便性状改变(变细、血便、黏液便等) l腹痛或腹部不适
—腹部肿块
—肠梗阻相关症状
—贫血及全身症状:如消瘦、乏力、低热等

PART2 病理分型
以病理组织学检查为依据,根据WHO分型系统,结直肠癌可分为:
—普通类型腺癌
—特殊类型腺癌:筛状粉刺型腺癌、髓样癌、微乳头状癌、黏液腺癌、锯齿状腺癌、印戒细胞癌
—少见类型癌:腺鳞癌、梭形细胞癌、鳞状细胞癌、未分化癌
—其他类型癌
—其中黏液腺癌、印戒细胞癌、未分化癌的恶性程度高
PART3 临床分期及预后

01.临床分期
结直肠癌的TNM分期系统
最常用来对结直肠癌进行分期的系统是美国癌症联合委员会(AJCC)的TNM分期系统。在TNM分期系统中,医生使用体格检查、活检和影像检查等的结果来回答TNM分期中的3个关键问题:
肿瘤(T):原发肿瘤在哪里,扩散到肠壁和临近器官有多深?
淋巴结(N):肿瘤是否扩散到淋巴结?如果有的话,扩散到了哪里的淋巴结和影响到了多少淋巴结?
转移(M):癌症已经转移到身体的其他部位吗?
原发肿瘤 (T)
描述了癌症在肠壁5层浸润的程度:
Tis 原位癌,局限于上皮内或侵犯黏膜固有层
T1 肿瘤侵犯黏膜
T2 肿瘤侵犯固有肌层
T3 肿瘤穿透固有肌层到达浆膜下层,或侵犯无腹膜覆盖的结直肠旁组织
T4a 肿瘤穿透腹膜脏层
T4b 肿瘤直接侵犯或粘连于其他器官或结构
区域淋巴结(N)
描述了淋巴结受累的程度:
N1 有1-3枚区域淋巴结转移
N1a 有1枚区域淋巴结转移
N1b 有2-3枚区域淋巴结转移
N1c 浆膜下、肠系膜、无腹膜覆盖结肠/直肠周围组织内有肿瘤种植, 无区域淋巴结转移
N2 有4枚以上区域淋巴结转移
N2a 4-6枚区域淋巴结转移
N2b 7枚及更多区域淋巴结转移
远处转移(M)
描述了远端转移的情况:
M1 存在一个或多个远隔部位、器官或腹膜的转移
M1a 远处转移局限于单个转移部位或器官,无腹膜转移
M1b 远处转移局限于两个及以上的转移部位或器官,无腹膜转移
M1c 腹膜转移,伴或不伴其他部位或器官转移
结直肠癌的TNM分期组合
一旦确定了T、N和M,就将这些信息组合并使用数字0和罗马数字I到IV来表示一个分期,这称为分期组合。某些分期会有进一步的亚分期,通过字母来表示,如IIA和IIB都是II期。举例,如果一个患者是T4a、N2a、M0,对应具体的肿瘤分期就是ⅢC期。
Ⅰ期
侵犯粘膜或基层,无淋巴结转移
Ⅱ期
侵犯外膜或浆膜,无淋巴结转移
Ⅲ期
已经有局部淋巴结转移,术后复发风险高
Ⅳ期
出现了远端转移
结直肠癌转移途径,1.局部扩散(壁内环形,纵行扩散,壁外蔓延);2.淋巴道扩散;3.血道扩散:肝脏最常见;4.种植转移(粘膜面,浆膜面)
02.预后
结直肠癌预后主要和分期相关,一般Ⅰ期的结直肠癌五年生存率大概是80%-90%,Ⅱ期的结直肠癌五年生存率在70%左右,Ⅲ期的五年生存率一般在30%-50%,Ⅳ期的五年生存率一般在10%左右
PART4 治疗与基因检测
目前肿瘤的主要治疗方法包括:手术治疗、放射治疗、化学药物、靶向药物、免疫治疗和联合治疗。2015年1月20日,美国总统奥巴马在国情咨文中宣布“精准医疗计划”,标志着精准医疗时代的到来,精准医疗就是指根据患者的基因检测结果给予相匹配的靶向/免疫治疗策略。
根据CSCO指南和NCCN指南:
IA、IB期结直肠癌患者给予手术治疗即可,无须术后辅助治疗;
IIA、IIB期结直肠癌患者以手术治疗为主,高危患者术后需要辅助治疗,推荐进行MSI-H/dMMR的检测, MSI-H/dMMR型患者预后较好,但不能从术后5-FU辅助治疗中获益;
IIIA-IIIC期结直肠癌患者主要是术前同步放化疗+手术+辅助化疗,指南里并未推荐进行基因检测;
Ⅳ期结直肠癌患者指南里推荐进行KRAS、NRAS、BRAF等基因的检测,并且根据具体的检测结果给予对应治疗。
指导靶向、免疫治疗用药
以KRAS、NRAS和BRAF的检测结果为例,如果这三个基因均是野生型,可以推荐使用两药或三药化疗(5FU/奥沙利铂、卡培他滨、伊立替康)±西妥昔单抗/帕尼单抗(左半结肠癌),患者PFS( 无进展生存期)和OS(总生存期)均有受益,其他基因对应治疗方案详见下表。
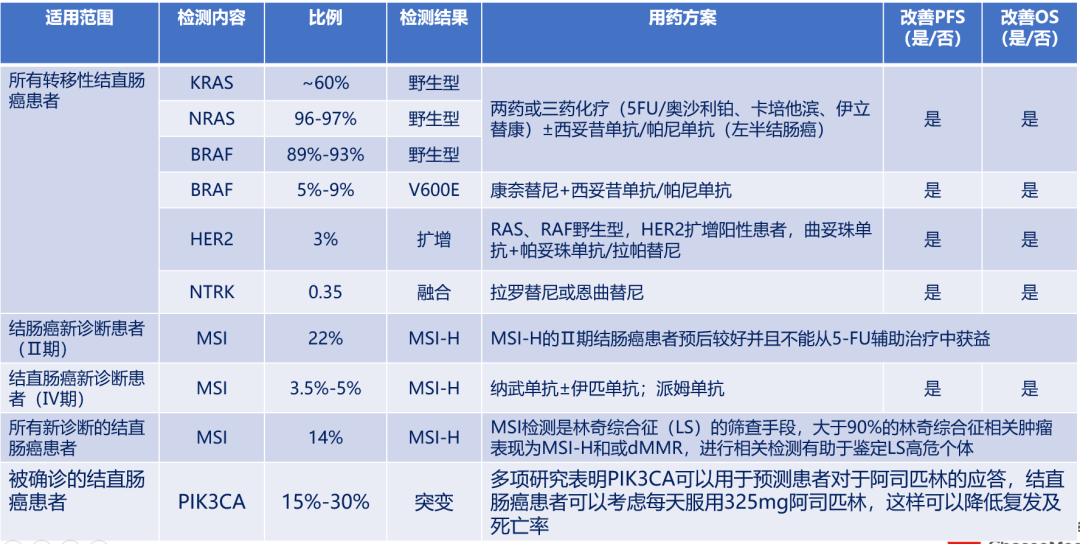
指导化疗用药
伊立替康和氟尿嘧啶是结直肠癌常用的化疗药物,现有研究结果表明UGT1A1*28等位基因的存在可导致伊立替康活性代谢产物SN-38的显著增加,从而发生腹泻/中性粒细胞减少的几率显著增加,因此建议该基因纯合型患者每3周最大输注剂量降低至400mg。接受氟尿嘧啶类药物治疗的患者,需要考虑DPYD的基因状态,并根据突变状态给予合适的药物剂量。
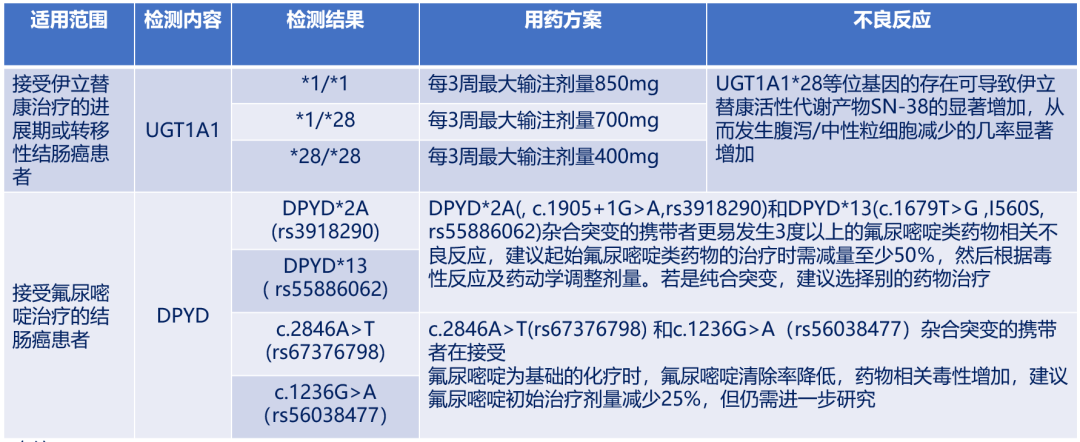
评估遗传风险
遗传性肿瘤是指由特定致病基因突变导致并具有家族聚集性的肿瘤类型,约占癌症的5-10%。遗传性肿瘤具有如下特征:发病年龄轻、成对器官的双侧肿瘤,如双侧乳腺癌,双侧肾癌、无外环境风险因素出现、多发原发性肿瘤、有家族史和罕见肿瘤。

与遗传性结直肠癌相关的综合征有很多,以林奇综合征(LS)为例,该综合征由EPCAM, MLH1,MSH2, MSH6和PMS2的胚系致病性突变相关,患CRC等多种恶性肿瘤的风险增加,有这些基因突变导致的结直肠癌占总患者群体的2-4%。针对于LS个体,结肠癌的风险管理措施:
从20-25岁开始进行结肠镜检查(如果是MSH6致病性突变,可以适当延迟结肠镜检查时间,比如从30岁开始,如果家族中有亲属罹患结肠癌需早于被确诊亲属发病年龄的10年开始结肠镜检查;PMS2的数据较少,暂时没有明确的结肠镜检查起始年龄推荐),如果最早的结肠癌患者早于25岁被确诊,建议早于确诊年龄的2-5年开始,每1-2年进行结肠镜检查(包含有结直肠癌家族史,性别为男性,携带MLH1/MSH2致病性突变,年龄大于40岁,有腺瘤史这些危险因素的个体更容易从每年的筛查中获益),有数据支持阿司匹林可以降低LS综合征患结肠癌的风险,但是合适的剂量和用药时间不明确。
总结
基于NGS的结直肠癌基因检测可以做到ALL IN ONE,一次检测提供多种提示信息:
1. 指导结直肠癌患者靶向药物选择,如靶向药西妥昔单抗只适用于KRAS、NRAS和BRAF野生型患者
2. 指导结直肠癌患者免疫药物选择,如免疫治疗药物适合dMMR/MSI-H型患者
3. 指导结直肠癌患者化疗药物选择,如UGT1A1*28等位基因的存在使得伊立替康毒副作用增加,因此应降低药物使用剂量
4. 提示结直肠癌患者家族遗传风险,如携带MLH1基因胚系致病性突变个体,患结直肠癌风险增加,应加强筛查,早发现早治疗,争取最佳预后