学习免疫治疗新知识、新理念,全面迎接中国食管癌诊疗新时代。
食管癌是全球常见的消化道肿瘤之一,在我国,每年新发和死亡人数约占全球一半以上,是食管癌的重灾区。近年来,免疫治疗不断取得突破,在食管癌治疗中也占据越来越重要的地位。为规范食管癌诊疗,向中国临床医生传递国内外免疫治疗的各种新数据、新理念以及新治疗方案,中国抗癌协会(CACA)发起“2020年食管癌诊疗规范行”项目,为全国同行搭建一个互相交流的线上学习交流平台。
“2020年食管癌诊疗规范行”自 8月27日正式拉开帷幕,共计开展20个专场,上百位食管癌领域专家齐聚云端,共同促进食管癌的诊疗规范化。截至目前“2020年食管癌诊疗规范行”已开展6个专场,线上线下吸引了众多专家学者,每个专场都可谓是食管癌领域的饕餮盛宴,下面就让我们来一同感受高端学术的魅力吧!
晚期食管癌一线治疗新进展
大多数中国食管癌患者就诊时已处于中晚期,且组织学类型90%以上为食管鳞癌,预后更差。历经半个多世纪的发展,晚期食管癌的治疗选择仍然非常有限。化疗是目前东西方指南对局部晚期或转移性食管癌推荐的一线标准治疗方案,但有效率较低,约38%-42%,中位总生存期也仅12.67-13.46个月,且3级以上不良反应较高,达68.6%-81%。
近年来研究发现,食管癌是一种免疫原性强的肿瘤类型,PD-L1表达较高,为食管癌免疫治疗探索提供了理论基础。2019年,KEYNOTE-181、ATTRACTION-3、ESCORT三大研究结果相继发布,一致显示免疫治疗相比化疗具有优效性,确立了免疫治疗在食管癌中二线治疗的地位。2020美国国家综合癌症网络(NCCN)指南和2020中国临床肿瘤学会(CSCO)指南也对免疫治疗进行了更新,均推荐帕博利珠单抗作为PD-L1 CPS≥10的晚期食管鳞癌患者的二线治疗方案,标志着我国食管癌治疗进入了免疫时代。而免疫检查点抑制剂二线治疗的成功也有力推动了前移至一线治疗的探索。
2020欧洲肿瘤内科学会(ESMO)大会上公布了KEYNOTE-590研究结果,这是全球首个免疫一线治疗局部晚期或转移性食管癌的III期临床研究。KEYNOTE-590共入组749例未曾接受药物治疗的不可切除局部晚期或转移性食管癌患者,随机给予帕博利珠单抗+顺铂+5-氟尿嘧啶(5-FU)和顺铂+5-FU一线治疗。结果显示,帕博利珠单抗联合化疗一线治疗组患者客观缓解率(ORR)(研究者评估)达45%,相比化疗组(29.3%)显著提高(P<0.0001)。
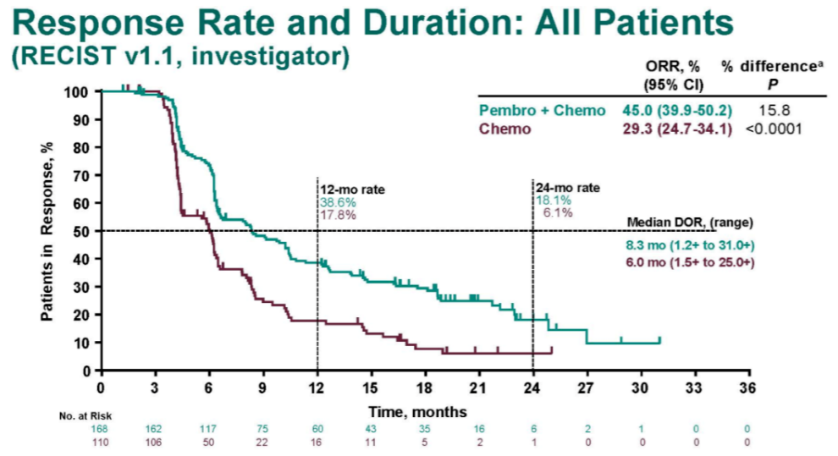
整体人群ORR
无论是在ITT人群,还是食管鳞癌(ESCC),或PD-L1 CPS≥10的ITT和 ESCC人群中,K药联合化疗一线治疗在总生存期(OS),无进展生存期(PFS),ORR和持续缓解时间(DOR)数据上显示了相比单纯化疗一线治疗显著的优越性,安全性数据则与标准化疗相当。
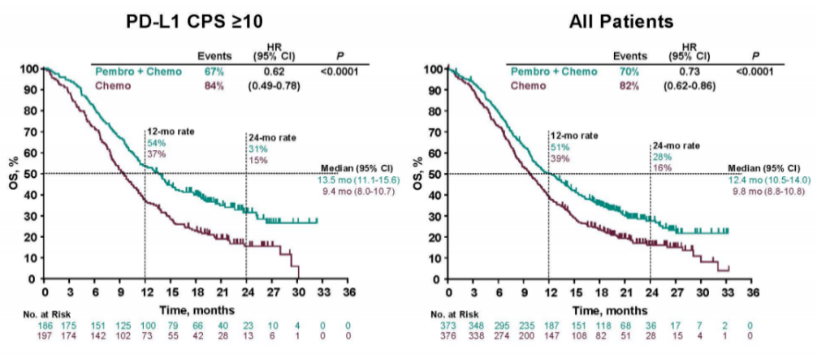
PD-L1 CPS≥10患者OS和整体人群OS
专家们在讨论中指出,KEYNOTE-590在研究设计上全面考虑了东西方人群的差异性、以及病理类型的差异,对不同病理类型(腺癌或食管鳞癌)、地域(亚洲或非亚洲人群)、PD-L1表达情况做了分层分析,而且它还结合病理类型和PD-L1表达情况增加了一组PD-L1 CPS≥10的食管鳞癌人群的分析。四个亚组分析中,帕博利珠单抗联合化疗相比化疗可全面提高近期和远期疗效。免疫联合化疗将改变晚期食管癌一线治疗临床实践和指南。
局部晚期食管癌免疫治疗新进展
局部晚期食管癌的治疗主要有可切除(手术)和不可切除(根治性放化疗)两种治疗模式,然而单一手术治疗后患者中位OS不足25个月,且30/90天死亡率高,如何提高围手术期的治疗效果和患者生存一直是临床医生面临的问题。
多项临床研究显示,术前新辅助放/化疗相比单一手术可延长局部晚期食管癌患者的无病生存期(DFS),提高整体生存率,降低死亡风险。CROSS研究显示,相比单一手术治疗,术前新辅助放化疗可延长患者OS,奠定了同步放化疗在新辅助治疗中的地位。
随着免疫治疗的出现,人们开始探索术前新辅助治疗加入免疫治疗是否可进一步延长患者生存。临床前研究显示,免疫治疗可协同化疗促进肿瘤细胞凋亡,并且消除放疗微环境的免疫抑制因素,改善放疗敏感性,提示免疫联合放/化疗具有1+1>2的效果。
PERFECT研究证实,新辅助放化疗联合阿替利珠单抗治疗可切除食管腺癌患者病理完全缓解(pCR)率达39%,3-4级不良反应发生率为48.4%。NCT03044613研究证实纳武利尤单抗联合同步放化疗新辅助治疗Ⅱ/Ⅲ期食管/胃食管交界处癌Ⅰb期患者pCR率为40%,不良反应可接受,无手术延迟。2019ASCO发布的新辅助放化疗联合Avelumab治疗可切除的局部晚期食管及食管胃交界癌pCR率达43%。2019ESMO发布的Ⅱ期研究显示,新辅助放化疗联合帕博利珠单抗治疗局部晚期食管鳞癌原发灶pCR率达46.1%,1年OS达82.1%。
四川省人民医院的曾铭教授指出:新辅助治疗有助于提高手术成功率,目前有关免疫新辅助的探索研究多数处于Ⅰ/Ⅱ期阶段,局部晚期食管癌的免疫新辅助治疗仍有许多问题需要解决。免疫新辅助治疗为食管癌的治疗提供了一个新的选择,未来值得期待。
免疫疗效最佳预测指标,仍需不断探索
免疫治疗为食管癌患者带来曙光的同时,也正不断向精准治疗迈进,而精准治疗的实现离不开各类临床生物标记物。目前免疫治疗生物标记物分析主要集中在肿瘤细胞特征和肿瘤微环境中的免疫细胞。
PD-L1是常见的免疫生物标记物,PD-L1表达水平评估在目前临床研究中应用最为广泛。KEYNOTE-059研究分析显示,相比TPS,CPS可以更好地确认缓解人群。KEYNOTE-062进一步分析显示,CPS表达高低与治疗预后呈正相关趋势。KEYNOTE-180对CPS界值进行了分析,结果显示将10分作为界值,可以最好地平衡阳性预测值、敏感性和阳性率。基于KEYNOTE-180结果,KEYNOTE-181增加了CPS≥10的研究终点分析,再次验证CPS≥10可以作为晚期二线食管癌免疫治疗的生物标记物。除帕博利珠单抗以外,CheckMate-032研究也证实,与TPS相比,CPS较高时,对OS的区分更显著。KEYNOTE-590研究也证实,CPS≥10 的PD-L1高表达食管癌患者有更好的获益趋势,PD-L1表达可作为预测免疫治疗获益的生物标记物。
除PD-L1表达水平以外,高微卫星不稳定性或错配修复缺陷(MSI-H/dMMR)和肿瘤突变负荷(TMB)也是肿瘤领域常用的疗效预测标记物。有研究显示,MSI状态可预测局部晚期可切除胃腺癌患者的生存获益。但MSI-H在食管癌中发生率较低,MSI可能是潜在的获益生物靶标,但是在局部晚期食管癌中的应用价值仍需临床数据进一步证实。
研究显示,TMB和T细胞炎症基因表达谱(GEP)在PD-1抗体的应答者和无应答者中表现出联合预测效用。TMB、预计CD+8T细胞丰度和PD-1 mRNA高表达片段组成的三变量模型显著提高不同癌种中的PD-1/PD-L1治疗的应答预测潜力。ESCORT I期试验显示,TMB高的患者对于免疫检查点抑制剂的有效率似乎更佳,但针对TMB的治疗目前尚无统一的判断标准。
未来展望
KEYNOTE-181、ATTRACTION-3、ESCORT三大研究阳性结果,奠定免疫治疗在食管癌中二线治疗的地位,寻找精准人群仍然是未来持续探索的方向。而KEYNOTE-590显示免疫联合化疗一线治疗患者获益更多,无新增不良反应,帕博利珠单抗联合化疗有望改写食管癌的一线治疗格局。未来,免疫单药、免疫联合化疗是否可以采用紫杉类药物代替顺铂以及免疫治疗获益人群的寻找值得进一步探索。
过去的两个月,“2020年食管癌诊疗规范行”已顺利开展多场线上学术会议,更多免疫治疗新知识、新进展的传递和交流仍在火热进行中,敬请关注!