目前,胆道肿瘤(BTC)的预后仍然很差,急需新的治疗策略来提高生存率。而随着首款靶向FGFR药物Pemigatinib的获批,更多针对靶点的研究也在大力开展中。最近对BTC的基因组分析显示,在近40%的患者中观察到几种潜在的靶向性基因改变,包括BRCA1/2突变。BRCA1/2突变表现出基因组不稳定性,增加了恶性转化的易感性。
今天小编就和大家分享一项ESMO上的研究,这是迄今为止研究BTC中BRCA突变状态与肿瘤突变负荷(TMB)关系的样本量最大的研究。此外,还包括BRCA突变与错配修复(MMR)/微卫星不稳定性(MSI)状态和PD- L1过表达之间的关系。

2018首发初期结果:I药单药挑战NSCLC三线+ 意外收获EGFR/ALK+免疫疗效
2018年The Lancet Oncology上发表了一项2期临床研究 ATLANTIC评估了PDL1 单抗Durvalumab(I药)单药用于三线及以上NSCLC治疗的疗效。

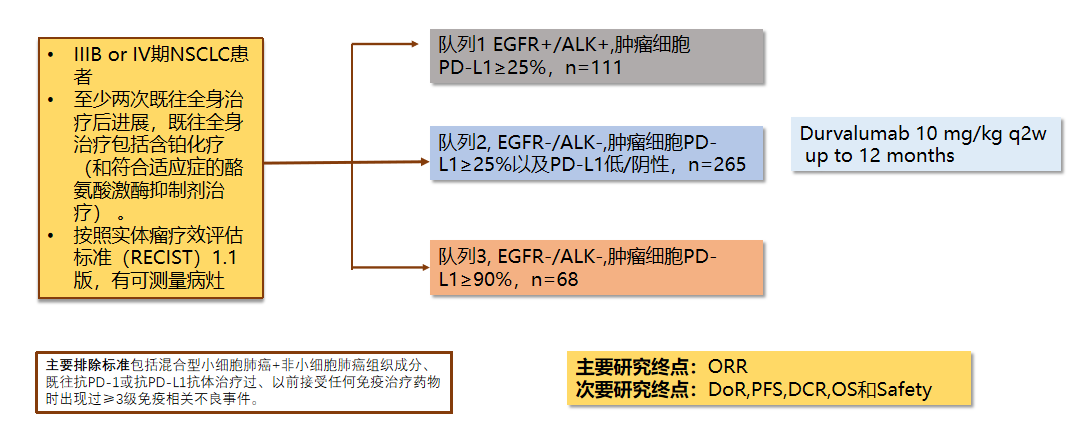
研究纳入IIIB或IV期经过至少两线治疗的NSCLC,给予I药单药治疗,根据PDL1表达情况和EGFR/ALK情况分为三个队列:①EGFR+/ALK+,PDL1≥25%;②EGFR/ALK阴性,PDL1表达不限;③EGFR/ALK阴性,PDL1≥90%。
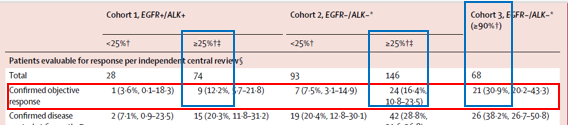
结果达到主要研究终点:队列2的ORR16.4%,队列3的ORR可以高达30.9%。在EGFR/ALK+的队列1中,PDL1≥25%的患者在后线治疗也有12.2%的有效率。
ATLANTIC结果的公布,印证了I药在非小细胞肺癌中的后线有效率,同时也为EGFR/ALK靶向治疗耐药后免疫使用增添一抹亮色。2018年数据公布时,研究中位OS尚未达到。
2020:OS结果公布,填补免疫后线空白,多个数据新颖,提出惊艳结论
今日,国外权威杂志LUNG CANCER公布了ATLANTIC研究II期试验数据[2],令人期待已久的OS数据也终于与大家见面了。

截至文章截稿,444名患者中有328名(73.9%)死亡。大多数死亡(306, 93.3%)是由疾病进展导致的。
OS数据:
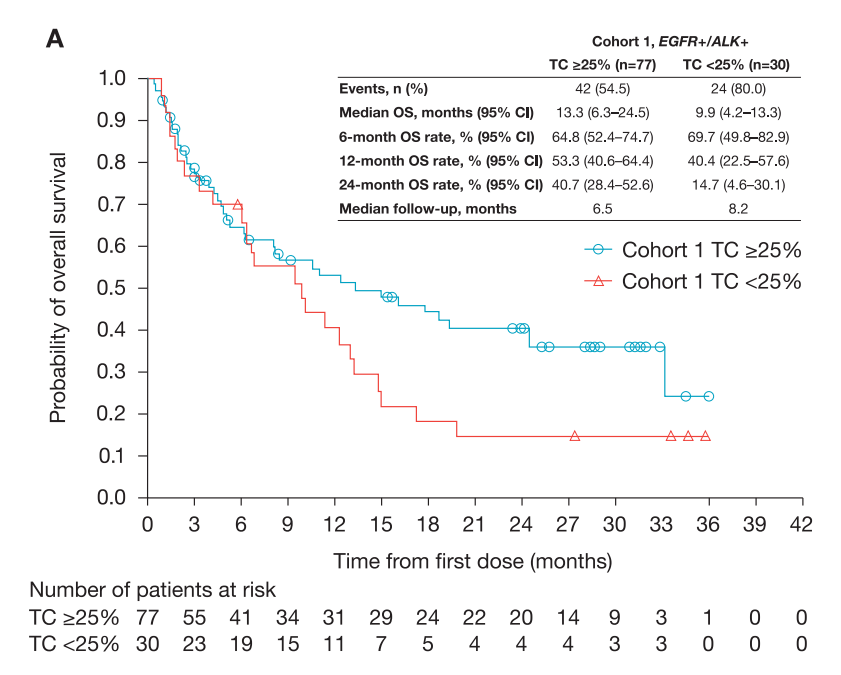
(1)队列一中,对于EGFR+/ALK+患者,PD-L1≥25%患者mOS为13.3个月,12个月OS率为53.3%,24个月OS率为40.7%;PD-L1<25%患者mOS为9.9个月,12个月OS率为40.4%,24个月OS率为14.7%。
有意思的是,对队列1中PD-L1≥25%的患者分为EGFR +或ALK + NSCLC进行探索性分析显示,ALK +亚组mOS为6.3个月(95%CI ,0.9,NR),EGFR +组中位OS的数值更长为16.1个月(95%CI 6.2-33.2)。 同样,EGFR + NSCLC患者的12个月OS率高于ALK + NSCLC患者。ALK阳性患者的免疫疗效较差,明显低于EGFR组。
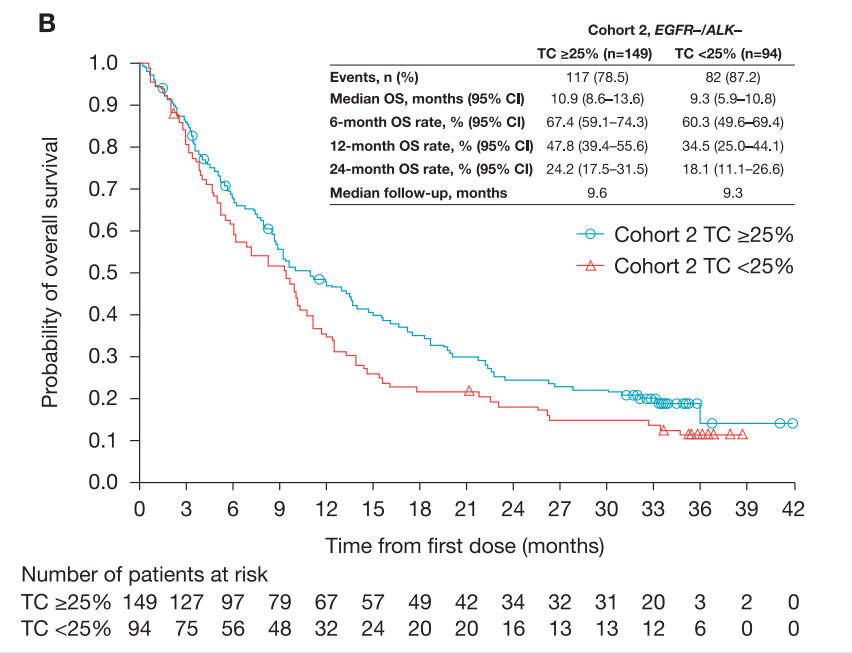
(2)队列二中,对于EGFR-/ALK-患者,PD-L1≥25%患者mOS为10.9个月,12个月OS率为47.8%,24个月OS率为24.2%;PD-L1<25%患者mOS为9.3个月,12个月OS率为34.5%,24个月OS率为18.1%;
(3)队列三中,对于EGFR-/ALK-、PD-L1≥90%患者,mOS为13.2个月,12个月OS率为51.8%,24个月OS率为39.1%。
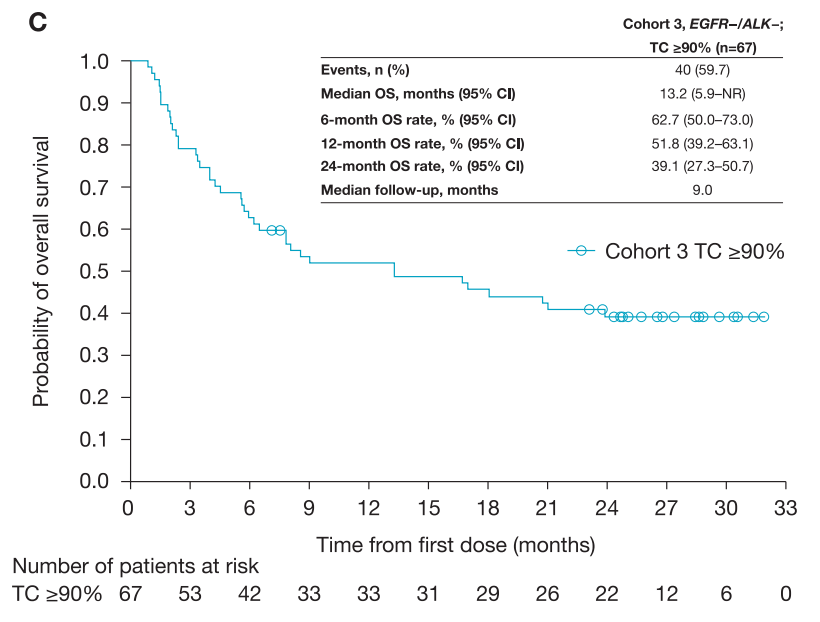
不管EGFR / ALK状态如何,PD-L1表达较高(PD-L1≥25%和PD-L1≥90%)的患者OS比PD-L1<25%更长。同样,PD-L1表达较高的患者,无论EGFR / ALK状态如何,其12个月和24个月OS率均升高。
03 后线安全性仍然较高!
本次公布的安全性数据也不负众望。444名患者中,有42名(9.5%)发生了3/4级治疗相关不良反应(TRAE),有28名患者(6.3%)发生了严重TRAE(表1)。10例(2.3%)患者因TRAEs发生导致治疗终止。没有因TRAE引起的死亡,但在随后的EGFR-TKI治疗后有因肺炎导致的死亡。
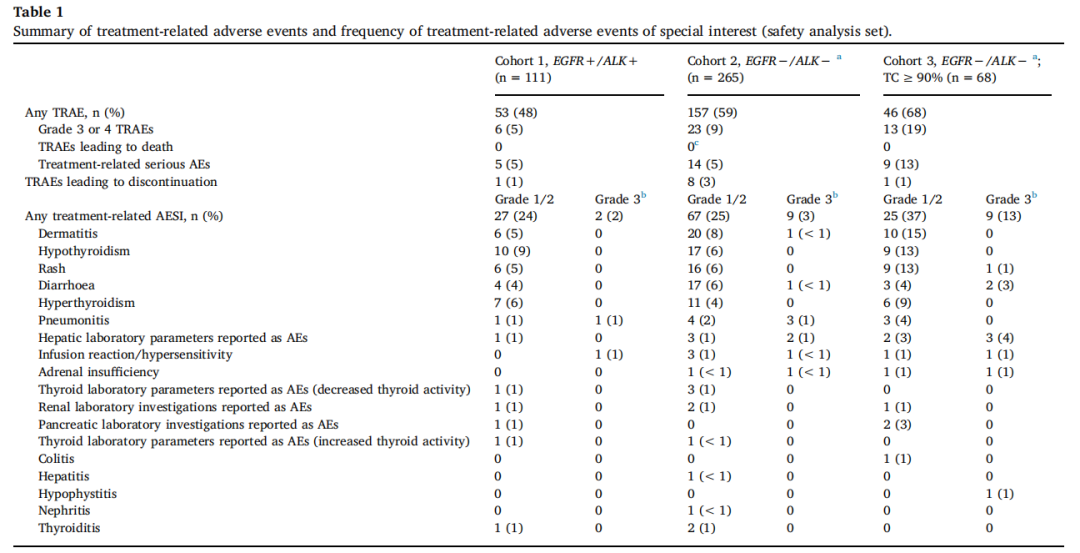
总共444例患者中有139例(31.3%)患有与治疗相关的有特殊意义的不良反应(AESI)。
队列1中有29(26.1%),队列2中有76(28.7%),队列3中34(50.0%)(表1)。最常见的与治疗相关的AESI是皮炎(37例,8.3%),甲状腺功能低下(36例,8.1%),皮疹(32例,7.2%),腹泻(27例6.1%)和甲亢(24 例,5.4%)。
与治疗有关的最常见的3级AESI是肝脏不良反应(5例,1.1%),肺炎(4 例,0.9%),腹泻(3例,0.7%)和输注反应(3 例,0.7%)。没有4/5级与治疗相关的AESI。队列3的治疗相关AESI发生率高于队列1和2。
总结
ATLANTIC研究的成熟的最终OS数据令人鼓舞,在经多线治疗的NSCLC患者中,durvalumab显示出很好的临床效应。毒性低,安全可靠,也为我们提供了很多新的临床免疫用药结论。
(1)ATLANTIC是迄今为止对EGFR + / ALK + NSCLC(n = 111)患者进行抗PD-1 / PD-L1治疗的最大前瞻性分析。对于EGFR / ALK阳性的患者,特别是PDL1≥25%的患者组,mOS可以达到13.3个月,12个月OS率为53.3%,24个月OS率为40.7%。高于EGFR/ALK阴性PDL1≥25%的患者组(mOS为10.9个月,12个月OS率为47.8%,24个月OS率为24.2%),甚至与EGFR/ALK阴性PDL1≥90%患者组(mOS为13.2个月,12个月OS率为51.8%,24个月OS率为39.1%)相当。即使,EGFR/ALK阳性PDL1<25%的患者组,OS数据也并不没有低于其他低表达组整体水平(mOS为9.9个月,12个月OS率为40.4%,24个月OS率为14.7%)。否定了既往EGFR/ALK阳性患者不适合使用免疫的结论。靶向化疗耐药后线序贯免疫仍是可行的。
(2)PDL1的疗效预测能力肯定。不论EGFR / ALK状态如何,肿瘤PD-L1表达较高的患者的mOS更长,对于PD-L1表达较低的患者,mOS高于9个月,提示无论前线后线使用免疫,适时检测PDL1,仍然可以起到很好的免疫疗效预测作用。
(3)疗效与不良反应成正比?福祸相依。虽然PDL1高表达患者OS获益更明显,但是PDL1≥90%的队列3的治疗相关AE发生率高于队列1和2。但是AI可以通过标准指南进行管理,并且大多数严重性为1/2级。这些结果与在晚期NSCLC中进行的其他抗PD-1 / PD-L1药物一致[3,4]。也提示我们,虽然PDL1高表达的患者免疫治疗效果更优,但要格外注重不良反应的预防与管理。
(4)EGFR+后线免疫生存数据是ALK+患者的3倍。EGFR + NSCLC(PD-L1≥25%)的患者mOS为16.1个月,ALK + NSCLC的患者中位OS较短(6.3个月),EGFR + NSCLC(PD-L1≥25%)患者mOS近ALK + NSCLC的三倍。ALK靶点似乎并不适合免疫。当然作者也提及本研究中ALK阳性组只有12名患者,样本量小,需要大数据人群验证该结论。
总之,ATLANTIC研究的最终OS数据再次为durvalumab在经治晚期NSCLS患者的疗效,填补了免疫后线的肺癌治疗数据空缺。且获得重要结论,在EGFR +非小细胞肺癌患者中,依然能获得不输EGFR阴性患者的生存数据。打破了“ EGFR + / ALK +不能从免疫治疗中获益”的传统认知,是免疫治疗在EGFR + / ALK +的初探索,也为晚期NSCLS的治疗,尤其为TKI耐药后的治疗带来了新的希望。
参考文献
[1]https://www.thelancet.com/pdfs/journals/lanonc/PIIS1470-2045(18)30144-X.pdf
[2]Marina Chiara Garassino,et al.,Final overall survival and safety update for durvalumab in third- or later-line advanced NSCLC: The phase II ATLANTIC study,[J]Lung Cancer 147 (2020) 137–142
[3]R.S. Herbst, P. Baas, D.W. Kim, et al., Pembrolizumab versus docetaxel for previously treated, PD-L1-positive, advanced non-small-cell lung cancer (KEYNOTE-010): a randomised controlled trial, Lancet 387 (10027) (2016) 1540–1550,
[4]]A. Rittmeyer, F. Barlesi, D. Waterkamp, et al., On behalf of the OAK Study Group. Atezolizumab versus docetaxel in patients with previously treated non-small-cell lung cancer (OAK): a phase 3, open-label, multicentre randomised controlled trial,Lancet 389 (10066) (2017) 255–265,
[5] O. Bylicki, N. Paleiron, J. Margery, et al., Targeting the PD-1/PD-L1 immune checkpoint in EGFR-mutated or ALK-translocated non-small-cell lung cancer,Target. Oncol. 12 (5) (2017) 563–569.
[6] R.A. Soo, S.M. Lim, N.L. Syn, et al., Immune checkpoint inhibitors in epidermal growth factor receptor mutant non-small cell lung cancer: current controversies and future directions, Lung Cancer 115 (2018) 12–20.