2019年对肿瘤患者而言是非常值得欣喜的一年。全球范围内批准了众多创新肿瘤药物和扩展了多款现有药物的适应证,大大丰富了肿瘤患者的药物选择,各项临床研究结果也相继出炉。接下来,我们就一起盘点下今年最具突破性的8项临床研究。
1 K药治疗NSCLC的5年生存率:KEYNOTE-001
就在几年前,非小细胞肺癌(NSCLC)几乎还是一个不治之症,5年生存率几乎不到5%。
2019年4月,免疫明星药物默沙东K药(帕博利珠单抗)再次被美国FDA批准,拿下一线治疗III期不适合手术切除或明确的化疗或转移性的NSCLC患者,TPS≥1%(TPS:只在肿瘤细胞中计算PD-L1表达评分)。而此前,FDA要求K药一线治疗NSCLC,必须TPS≥50%。
FDA之所以改变主意源于一项临床试验:KEYNOTE-001,这也是迄今为止帕博利珠单抗治疗晚期NSCLC患者的最长期随访研究。
2019年6月,ASCO大会披露了KEYNOTE-001的5年数据。研究显示:帕博利珠单抗单药治疗可显著提高晚期非小细胞肺癌(NSCLC)患者的总生存(OS)率。
该研究从2011年开始招募患者,共入组550例晚期NSCLC患者,其中未经治患者101例,经治患者449例。结果显示:18%的患者(100例)仍生存。初治患者5年OS率为23.2%,经治患者为15.5%,且PD-L1高表达患者的获益最大。
未经治患者中,PD-L1表达≥50%时,5年OS率为29.6%;PD-L1表达<50%者中则为15.7%;
经治患者中,PD-L1表达≥50%时,5年OS率为25%,PD-L1表达1%~49%患者为12.6%,PD-L1表达<1%者中仅为3.5%。
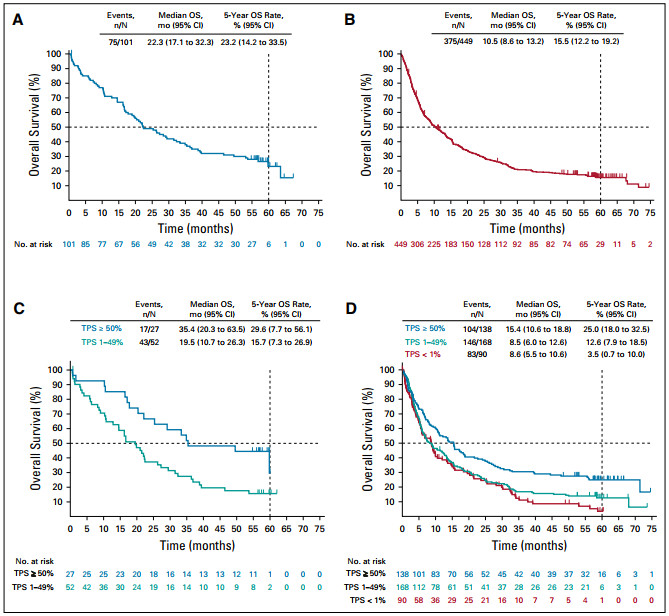
图1.5年OS率,来自KEYNOTE-001。A组为未经治患者,B组为经治患者,C组为未经治患者不同TPS,D组为经治患者不同TPS,其中TPS≤1%有12名患者。图片来自:doi:10.1016/S0140-6736(18)32559-5
KEYNOTE-001研究证实帕博利珠单抗用于初治患者5年OS率达23.2%,经治患者达15.5%,这项研究结果对于原先只有5%晚期NSCLC患者生存5年而言具有里程碑式的意义。
亚特兰大肿瘤研究所副主任Suresh Ramalingam表示:“(结果表明)临床上持久治疗是非常重要的。”凯特琳癌症中心专门研究肺癌的专家Mark G. Kris说:“这项研究揭示了一种可治愈转移性肺癌方案的潜力。”
2 O药联合Y药治疗晚期黑色素瘤:CheckMate 067
而作为K药的老对手,O药(纳武利尤单抗)在今年10月份《新英格兰医学杂志》也发布了一项重磅研究,进一步拓展了CheckMate 067临床试验结果。
CheckMate 067研究是一项双盲、随机、III期研究,在945例既往未接受治疗(初治)晚期黑色素瘤患者中开展,评估了纳武利尤单抗+Y药(Ipilimumab)组合疗法、纳武利尤单抗单药疗法相对于Ipilimumab单药疗法的疗效和安全性。
最新研究显示,在至少60个月的随访中:
中位OS:纳武利尤单抗+Ipilimumab组超过60.0个月(中位未达到),纳武利尤单抗组超过36.9个月,Ipilimumab组为19.9个月;
5年OS率:纳武利尤单抗+Ipilimumab组为52%,纳武利尤单抗组为44%,Ipilimumab为26%;
无进展生存(PFS):纳武利尤单抗+Ipilimumab组为11.5个月,纳武利尤单抗组为6.9个月,Ipilimumab组为2.9个月。
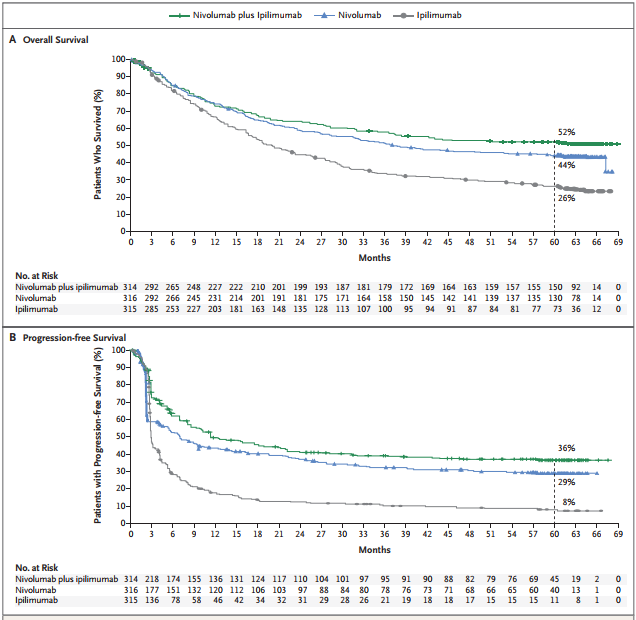
图2. 纳武利尤单抗+Ipilimumab、 纳武利尤单抗、Ipilimumab分组OS、PFS数据。图片来自:doi:10.1056/NEJMoa1910836
2018年,美国NCCN已经推荐纳武利尤单抗+Ipilimumab作为晚期黑色素瘤患者的一线选择。
“CheckMate 067研究已经改变了现有临床指南,而最新的5年随访数据的披露则让人进一步放心。”凯特琳癌症中心黑色素瘤专家Michael Postow表示,受益于纳武利尤单抗+Ipilimumab组疗效,超过50%的患者生存期超过5年。”这意味着通过免疫治疗,转移性黑色素瘤在大约一半的患者中不再有生命限制。“
3 新靶向联合治疗慢性淋巴细胞白血病
2019年5月15日,《新英格兰医学杂志》发布了一篇Ⅱ期研究,介绍了依鲁替尼联合B细胞淋巴瘤因子-2(BCL-2)抑制剂Venetoclax方案一线治疗高危慢性淋巴细胞白血病(CLL),试验结果非常惊艳,甚至可以让患者直接舍弃化疗。
该研究入组了80例初治的高危患者和老年患者,首先给予依鲁替尼单药疗法(420 mg/d)治疗3个周期,然后加入Venetoclax(每周剂量递增直至400 mg/d)联合治疗24个周期。
这些患者至少具备以下1种高危因素:染色体17p缺失、突变的TP53、染色体11q缺失、未突变的IGHV、65岁以上。
结果显示:在仅仅接受12个周期后,几乎90%的患者完全缓解(包括血液计数恢复不完全情况);61%的患者在未检测到微小残留疾病的情况下达到缓解;1年PFS率估计为98%,OS率为99%。
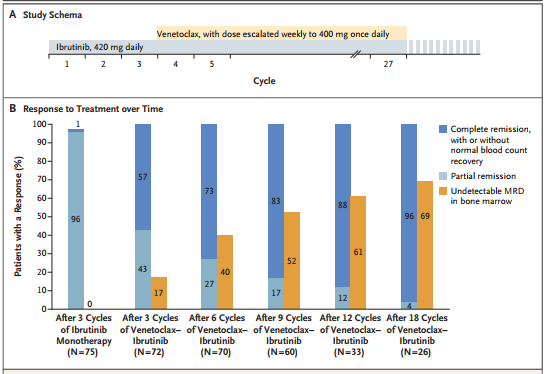
图3.依鲁替尼+Venetoclax联合治疗效果。图片来自:doi:10.1056/nejmoa1900574
虽然依鲁替尼联合Venetoclax方案还没有获批美国FDA,但是Venetoclax和其他单克隆抗体的联合使用方案已经有获批成功的例子:
2019年5月15日,美国FDA批准Venetoclax联合Obinutuzumab用于成人CLL或小淋巴细胞淋巴瘤(SLL)的初始治疗。
2018年6月18日,美国FDA批准Venetoclax联合利妥昔单抗治疗至少经过1种疗法的CLL或SLL。
威斯康星州医学院血液恶性肿瘤科主任Ehab Atallah教授表示:“这种非常有效的低强度联合疗法改变了我们目前对CLL患者的治疗方案,是该领域最具有影响力的发现之一。未来,Venetoclax联合其他单抗一线治疗CLL患者或许会惠及更多的患者。”
4 CDK4/6抑制剂治疗激素受体阳性晚期乳腺癌:MONARCH 2
在过去的两年里,美国FDA已经批准了三种CDK4/6抑制剂,研究也充分表明这些药物可以提高了激素受体阳性转移性乳腺癌患者的PFS率和生活质量。
2019年9月29日,《JAMA肿瘤杂志》三期临床试验MONARCH 2数据。
MONARCH 2是一个全球性的、双盲的III期临床试验,患者均为激素受体阳性(HR+)、人体表皮生长因子受体2阴性(HER2-)的晚期乳腺癌患者。
2014年8月至2015年12月间,669例患者被随机分配接受Abemaciclib+氟维司群(n=446)或安慰剂+氟维司群(n=223)。

图4.Abemaciclib+氟维司群、安慰剂+氟维司群整体OS。图片来自:doi:10.1001/jamaoncol.2019.4782
结果显示,Abemaciclib+氟维司群组中位OS为46.7个月,而安慰剂+氟维司群组为37.3个月。无论患者是否绝经,都能从Abemaciclib+氟维司群联合疗法中获益。
联合方案最常见的不良反应:中性粒细胞减少(29.9%)、腹泻(14.5%)、白细胞减少(11.1%)和贫血(9.1%)。
匹兹堡大学医学院医学教授Adam Brufsky博士说:“MONARCH 2试验进一步证明了CDK 4/6抑制剂在激素治疗中对晚期ER-阳性乳腺癌患者治疗的优越性。”他指出,最近的数据强调“这些组合现在应该被视为晚期ER-阳性乳腺癌的治疗标准。”
5 PARP抑制剂治疗前列腺癌:PROfound
“也许今年最激动人心的试验是首个以生物标志物为导向的治疗方法,用于治疗难治性的转移性前列腺癌。”克利夫兰诊所高级前列腺癌研究项目主任Jorge Garcia说。
2019年欧洲肿瘤医学会会议公布了PROfound试验数据。研究者在临床III期深入比较了PARP抑制剂奥拉帕利和新型激素治疗(恩杂鲁胺或者阿比特龙),并将400名DNA修复缺陷型转移性去势抵抗性前列腺癌患者分为两组:
A队列:有BRCA1、BRCA2或ATM基因的改变;
B队列:有12个已知参与DNA修复的其他基因中的任何一个的改变。
结果显示:
A队列中,使用奥拉帕利组的PFS为7.39个月,而使用激素治疗组的PFS为3.55个月,A组和(A组+B组)的PFS分别为5.8个月和 3.2个月。虽然死亡人数还不足得出确切的结论,但是A组中位OS显示:用奥拉帕利组为18.5个月,新型激素治疗组为15.11个月。
“这项研究对该领域的影响是巨大的。”Garcia补充道,这项试验强调了“肿瘤基因组学和生物标志物驱动的晚期前列腺癌临床研究的重要性。”
美国希望之城研究中心泌尿生殖系统癌症项目负责人Tanya Dorff博士认为,这项深度试验代表了前列腺癌治疗的重大转变。这项试验是第一个明确的1级证据表明,PARP抑制剂优于雄激素靶向治疗转移性去势抗性前列腺癌患者的DNA修复缺陷。
6 PARP抑制剂治疗卵巢癌:PRIMA
除了前列腺癌,PARP抑制剂在卵巢癌领域也大放异彩。无论是否检测到BRCA突变,其有望成为复发或新诊断的晚期卵巢癌患者最新选择。
2019年9月28日,PARP抑制剂尼拉帕利在《新英格兰杂志》公布了新诊断的卵巢癌患者中的3期数据。
研究者将733名对铂类化疗有反应的患者随机分为两组,一天服用一次尼拉帕利或安慰剂,为期36个月。结果显示,在对铂类化疗有反应的新诊断的晚期卵巢癌患者中,无论是否存在同源重组缺陷,接受尼拉帕利的患者比接受安慰剂的患者有更长的PFS。
尼拉帕利组和安慰剂组的总PFS分别为13.8个月和8.2个月,
同源重组缺陷患者对PARP抑制剂的反应更好,PFS为21.9个月,而安慰剂组为10.4个月。
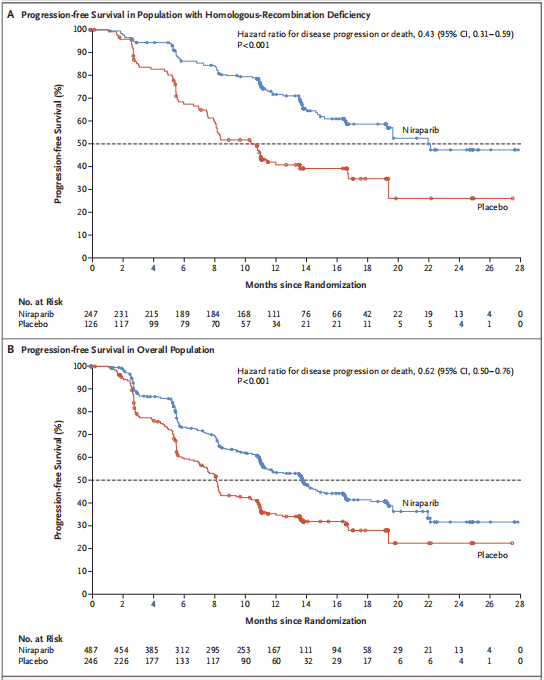
图5.尼拉帕利组和安慰剂组总体PFS对比。A组为同源重组缺陷人群的PFS,B组为PFS总人数。图片来自:10.1056/NEJMoa1910962
圣路易斯大学医学院妇科肿瘤学助理教授Shannon M.Grabosch说:“这个研究揭示了PARP抑制剂在维持卵巢癌PFS方面的潜力,改变卵巢癌一线维持(治疗)的可能性很大,尤其是无论BRCA在复发时状态如何,它都能显示出疗效。”
安德森癌症中心的妇科肿瘤学和癌症生物学教授Anil K. Sood认为,PARP抑制剂能帮助更广泛的患者,但同时他也注意到,如何区别特定亚组和全部患者群还需要对生物标记物进行进一步研究。
7 三联疗法治疗转移性结直肠癌:BEACON
在转移性结直肠癌(CRC)患者,有多达15%的患者存在BRAF V600E突变,这意味着更严重的疾病和更低的生存几率。寻找一种能够提高这类晚期CRC亚型患者生存的药物疗法一直是医疗界的一项挑战。
10月24日,发表在《新英格兰医学杂志》上的BEACON试验表明,三联疗法确实使这些患者的OS率提高。该试验比较了三联疗法(BRAF抑制剂Encorafenib、MEK抑制剂Binimetini、EGFR抑制剂西妥昔单抗)、双重治疗(Encorafenib和西妥昔单抗)以及两种常规化疗方案。
研究者将665名以前接受过治疗的患者随机分配。结果显示与化疗相比,三联疗法显著提高了患者的OS率。
中位OS方面,三联疗法患者组为9.0个月,双药治疗组为8.4个月,化疗组为5.4个月。基于这些数据,美国NCCN今年在转移性CRC治疗方案中增加了三联疗法。
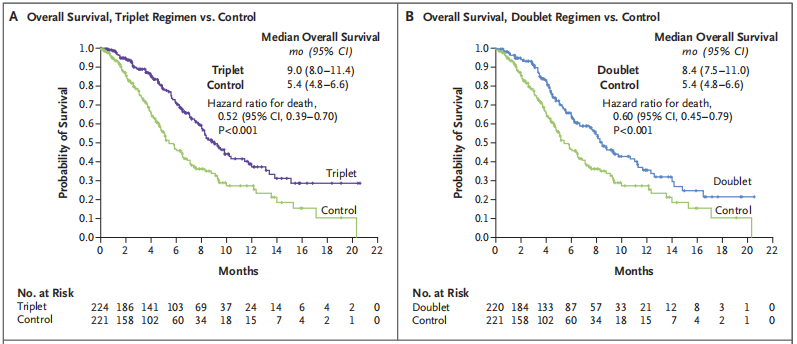
图6.三联疗法、双药治疗、化疗组OS对比。图片来自:10.1056/NEJMoa1908075
华盛顿乔治敦大学伦巴第综合癌症中心医学助理教授Benjamin Weinberg博士说:“三联疗法现在是首次接受化疗的患者首选的二线或后期治疗策略。这一选择很有吸引力,因为它使用了三种靶向药物,而且没有化疗。”
加州大学旧金山分校医学肿瘤学和转化研究杰出教授Alan P. Venook表示,毒性降低,生存率提高,这一疗法可能会成为新标准,但真正推广开来还需要更多讨论。
8 前列腺癌手术后跳过放疗:RADICALS-RT
前列腺癌患者术后应该接受放射治疗吗?这是一个困扰肿瘤学家多年的问题。目前,一项有史以来最大规模的前列腺癌术后放疗试验的数据有望能提供一些急需的参考。
在2019年欧洲肿瘤医学会会议上公布的Radiates-RT最新研究结果显示,男性在手术后通常可以免于放射治疗。Radiates-RT是前列腺癌术后放射治疗史上最大的试验,共招募了1396名接受前列腺癌术患者,他们被随机分配到术后放疗或仅采用标准的观察方法(如果复发则再接受化疗)。中位随访5年结果显示,放疗组PFS率为85%,标准治疗组为88%,两组的PFS率相似,几乎没有差异。
这项研究的第一作者、英国伦敦皇家马斯登国民保健基金会信托基金会和癌症研究所的Chris Parker教授说:“研究结果表明,术后应以观察为标准,只有癌症复发时才应使用放射治疗。在未来,许多男性将避免放疗的副作用,包括尿漏和尿道狭窄,这会使排尿困难。这两种都是单独手术后的潜在并发症,如果使用放射治疗,风险也会增加。”
根据泌尿生殖系统癌症专家Dorff的说法,在这项试验之前,肿瘤学家知道一些接受辅助放射治疗的男性不会从中受益。“通过追踪前列腺特异性抗原水平和治疗早期复发,我们现在可以省去一些不必要的治疗,这非常重要。”
参考文献
[1]. Garon E B, Hellmann M D, Rizvi N A, et al. Five-Year Overall Survival for Patients With Advanced Non‒Small-Cell Lung Cancer Treated With Pembrolizumab: Results From the Phase I KEYNOTE-001 Study[J]. Journal of Clinical Oncology, 2019: JCO. 19.00934.
[2]. Larkin J, Chiarion-Sileni V, Gonzalez R, et al. Five-year survival with combined Nivolumab and Ipilimumab in advanced melanoma[J]. New England Journal of Medicine, 2019, 381(16): 1535-1546.
[3]. Jain N, Keating M, Thompson P, et al. Ibrutinib and venetoclax for first-line treatment of CLL[J]. New England Journal of Medicine, 2019, 380(22): 2095-2103.
[4]. Sledge G W, Toi M, Neven P, et al. The effect of abemaciclib plus fulvestrant on overall survival in hormone receptor–positive, ERBB2-negative breast cancer that progressed on endocrine therapy—MONARCH 2: A Randomized Clinical Trial[J]. JAMA oncology, 2019.
[5]. Targeted Therapy Slows Progression of Advanced Prostate Cancer[ESMO 2019 Press Release]
[6]. González-Martín A, Pothuri B, Vergote I, et al. Niraparib in patients with newly diagnosed advanced ovarian cancer[J]. New England Journal of Medicine, 2019.
[7]. Kopetz S, Grothey A, Yaeger R, et al. Encorafenib, binimetinib, and cetuximab in BRAF V600E–mutated colorectal cancer[J]. New England Journal of Medicine, 2019, 381(17): 1632-1643.
[8]. Men with Prostate Cancer can be Spared Radiotherapy after Surgery[ESMO 2019 Press Release]
[9]. The 8 Most Notable Cancer Clinical Trials of 2019
*文章来源于 医学界肿瘤频道,版权归原作者所有,如有侵权请联系删除