
本文专家:
潘宏铭,浙江大学医学院附属邵逸夫医院肿瘤科学科带头人、主任医师,中国临床肿瘤学会肿瘤支持与康复专家委员会主任委员
厌食是人们日常生活中都可能遇到的问题,大部分是因为外界原因导致的压力、焦虑、抑郁、失眠或由于消化疾病引起的。
然而,厌食发生在肿瘤患者身上,一定不能大意!吃不下饭只是表象,长期存在或日趋加重的厌食,会导致患者无法耐受有效的抗肿瘤治疗,形成恶性循环,最终危害肿瘤患者的总生存期。
肿瘤患者的厌食会影响生存期
肿瘤患者厌食有一个专业名称,叫做癌性厌食,是肿瘤常见的伴随症状。
很多患者在进行治疗时,会感到吃不下饭,好像饭菜都不是原来的味道了,甚至伴有恶心呕吐。那么一定要注意,癌性厌食可能已经进展成肿瘤恶病质以厌食的“伪装”在攻击患者的身体。肿瘤恶病质的表现为早饱、味觉及嗅觉异常、食欲减退、恶心、呕吐、体重下降、肌肉和脂肪组织的消耗及其他胃肠道症状等[1]。
40%的初诊肿瘤患者初诊会出现癌性厌食,而中晚期肿瘤患者中的发生率高达80%[2]。癌性厌食会进一步导致肿瘤恶病质。2022年发表在精准营养杂志上的一项研究调查了我国16种常见肿瘤的47604例患者,有37.0%(17637例)出现肿瘤恶病质,其中胰腺癌患者患病率最高达63% [3]。恶病质在肿瘤早期就有较高概率发生,贯穿疾病全程,约20%的肿瘤患者直接死于恶病质造成的营养不良[4]。所以如何让肿瘤患者吃得下饭,维持身体的营养和机能,是抗肿瘤治疗中需要关注的问题。
浙江大学医学院附属邵逸夫医院肿瘤科学科带头人潘宏铭教授表示,“癌性厌食在肿瘤患者中发生非常普遍,进一步导致患者营养不良,发展为肿瘤恶病质,严重影响肿瘤患者的预后。我们应该在临床工作中早期识别癌性厌食,采取积极有效的多模式治疗方案,加强全程管理。希望更多的肿瘤患者和医生意识到癌性厌食-恶病质综合征治疗的必要性,通过协同努力进一步提升肿瘤患者的营养状态和临床预后,改善患者的生活质量,延长患者生存时间。”
肿瘤患者应对厌食做好这些事
1. 正确认识癌性厌食的危害
癌性厌食的发病机制较为复杂,肿瘤患者体内炎性因子分泌增加、肿瘤生长侵犯胃肠道、各类抗肿瘤治疗产生的毒副反应都会导致癌性厌食[5]。我们不能把厌食当作是患癌后正常的症状,单靠劝慰患者进食,结果是不尽如人意的,要关注到癌性厌食是需要治疗的疾病。
刊登于柳叶刀杂志的一项大型研究发现,对比食欲没有减退的肿瘤患者,完全没有食欲的患者生存时间缩短近5年![6]
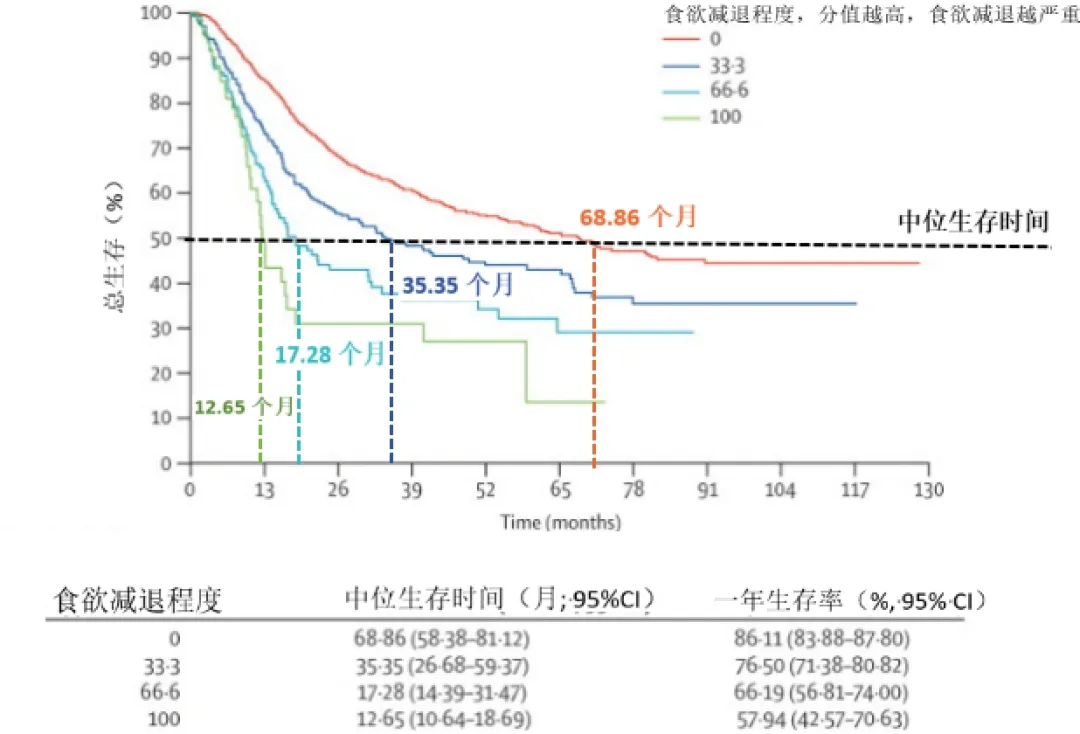
Lancet图
同时,医学家们通过对比体重和BMI指数发现,如果肿瘤患者体重丢失>5%,BMI<18.5,即使是最好的抗肿瘤治疗,其生存时间比体重正常(BMI≥22)的患者缩短3-5倍[7]。
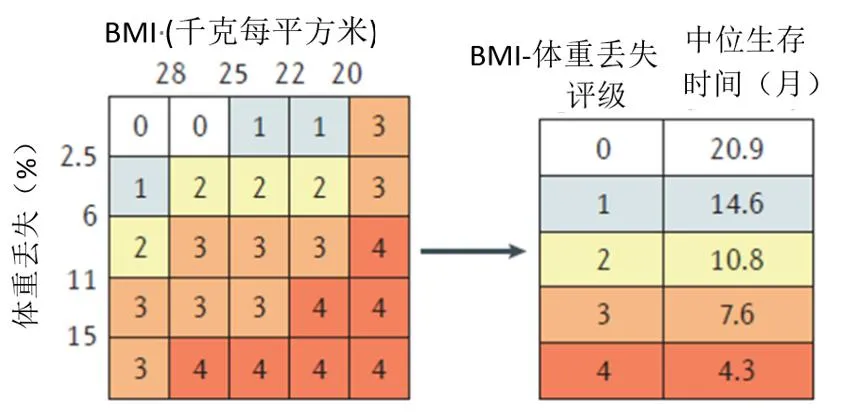
Eur J Cancer图
在肺癌治疗的过程中,一般认为患者至少需4个周期的化疗才能取得疗效,而肿瘤恶病质患者3个周期化疗的完成率降低了14%[8]。可见,肿瘤恶病质患者对治疗的耐受远不如其他患者,癌性厌食-恶病质综合征通过消耗患者肌肉、降低体重,使这些患者的治疗强度无法达到要求,疗效及生存时间大打折扣。
2. 关注肿瘤患者的这些指标,及早发现癌性厌食
从发现肿瘤的初期就关注患者的食欲和体重,对肿瘤恶病质的防治很重要。患者可以在日常生活中记录每天的食欲和体重的变化。一旦发现食欲明显下降,甚至体重下降的情况,应向医生求助,进行干预。
一旦在日常监测中发现问题,可以通过厌食/恶病质评价量表来评估厌食程度。该表每项评分为0-4分,总分48分。一般来说,如果整体评分≤37分,则可认定患有癌性厌食[9],需要积极治疗。
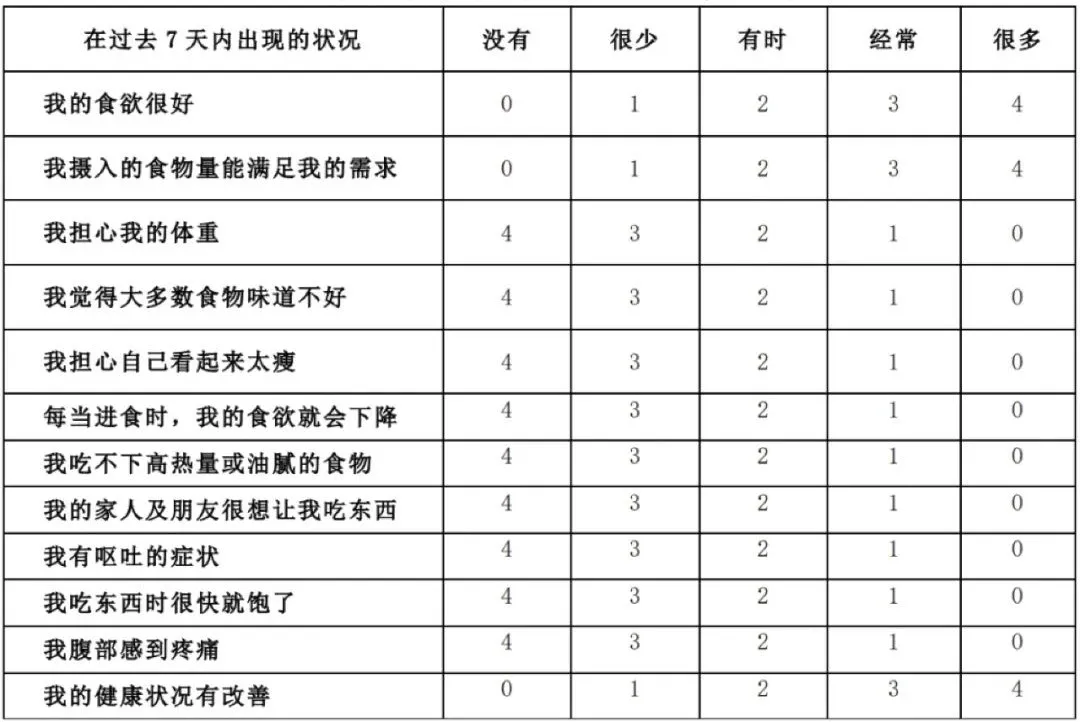
厌食/恶病质评价量表
有厌食症状的肿瘤患者还应密切关注C反应蛋白(CRP),它被认为是最实用的恶病质生物标志物。恶病质前期常出现CRP增高的现象,所以目前C反应蛋白>5毫克/升已经作为肿瘤恶病质的重要指标之一,但需要排除感染的可能性。
3. 及早干预,科学用药
多年来,国内外权威指南一致推荐甲地孕酮作为肿瘤患者改善食欲、治疗恶病质的首选药物。甲地孕酮通过刺激促食欲的神经元,提高中枢神经系统进食信号改善患者食欲。更重要的是,甲地孕酮具有抗炎作用,能够有效降低炎性因子的水平,从而阻止肌肉和脂肪组织的消解,使体重恢复,提升抗肿瘤治疗的疗效[10,11]。
然而,临床使用中发现甲地孕酮片剂的疗效个体差异大,有效率低。这是由于甲地孕酮不溶于水,很难被人体吸收。想要达到有效的吸收,须伴随高脂高热饮食(相当于30分钟内吃完2个煎鸡蛋、2根油条、240毫升全脂牛奶和100克火腿肠)[12-14],以此刺激胆汁大量分泌来解决甲地孕酮片剂的吸收障碍。但癌性厌食患者本身就没有食欲,几乎无法接受这样的饮食,极大地影响了甲地孕酮的疗效。
为了解决这个困境,国内不久前引进了纳米晶技术升级的醋酸甲地孕酮口服混悬液。通过将药物粒径研磨至纳米级别,大幅提高了甲地孕酮溶解度,能够快速达到疾病治疗所需的血药浓度。服用纳米晶型醋酸甲地孕酮口服混悬液的患者体重显著增加的时间从14天缩短至3天;在12周内平均体重增加5.4公斤,是普通剂型的1.5倍;增加的体重40%源于肌肉,60%源自脂肪[15]。患者可以在很短的时间内感受到食欲的改善,提升体重的效果大幅增加,有效延缓肿瘤恶病质的进程。
同时,很多研究证实,在抗肿瘤治疗的初期就关注患者的食欲情况并进行干预,患者的生存获益更显著。如果患癌后,在早期化疗时联合使用甲地孕酮,患者的中位生存时间对比单纯化疗可以延长近7个月[16]。此外,如果预防性地使用甲地孕酮治疗体重减轻比出现体重减轻的症状后再治疗,患者的体重减轻程度更小,生存更长时间[17]。
然而,很多人听到甲地孕酮是“激素”,不由自主地就联想到激素类药物的副作用。但醋酸甲地孕酮口服混悬液的安全性良好[18],属于羟孕酮类,无雌激素活性、具有抗雌激素效果,是血栓发生风险最低的一类孕激素[19]。一项针对甲地孕酮血栓风险的研究也佐证,患者使用甲地孕酮后并未增加血栓发生的风险[20]。但是,多数肿瘤患者属于血栓高风险患者,在使用甲地孕酮时应常规评估血栓发生风险,听从医生的专业意见,及时防治,更科学地用好甲地孕酮。
参考文献:
[1] 中国抗癌协会肿瘤营养专业委员会,肿瘤恶液质临床诊断与治疗指南(2020版),中国肿瘤临床,2021, 48(8)[2] VON HAEHLING S,et al. Prevalence,incidence and clinical impact of cachexia:facts and numbers-update 2014[J].J Cachexia Sarcopenia Muscle.2014;5(4):261-263.[3] Li X, Hu C, Zhang Q, et al. Cancer cachexia statistics in China[J]. Precision Nutrition, 2022, 1(1): 10.1097.
[4] Porporato PE. Understanding cachexia as a cancer metabolism syndrome. Oncogenesis. 2016 Feb 22;5(2):200.
[5] 黄蕾,金春晖. 癌性厌食发病机制的研究进展 [J].中国癌症防治杂志.2023;15 (04):423-428.
[6] Quinten C, et al. EORTC Clinical Groups. Baseline quality of life as a prognostic indicator of survival: a meta-analysis of individual patient data from EORTC clinical trials. Lancet Oncol. 2009 Sep;10(9):865-71.
[7] Andreyev HJ, Norman AR, Oates J, Cunningham D. Why do patients with weight loss have a worse outcome when undergoing chemotherapy for gastrointestinal malignancies? Eur J Cancer. 1998 Mar;34(4):503-9.
[8] Miyawaki T, Naito T, Yabe M, et al. Impact of weight loss on treatment with PD-1/PD-L1 inhibitors plus chemotherapy in advanced non-small-cell lung cancer. Support Care Cancer. 2022 Feb;30(2):1633-1641.
[9] Ribaudo JM, Cella D, Hahn EA.et al.Re-valiadation and Shortening of the the Functional Assessment of Anorexia/Cachexia Therapy(FAACT) Questionnaire. Qual Life Res. 2000,9(10):1137-1146.
[10] 齐玉梅,李增宁,李晓玲,等.肿瘤患者食欲评价和调节的专家共识[J].肿瘤代谢与营养电子杂志,2020,7(2):169-177.
[11] Argilés J M, Anguera A, Stemmler B. A new look at an old drug for the treatment of cancer cachexia: megestrol acetate[J]. Clinical nutrition, 2013, 32(3): 319-324
[12] FDA.Food Effect Working Group of the Biopharmaceutics Coordinating Committee, Office of Pharmaceutical Science.2009 2.
[13] 国家药品监督管理局.《新药研发过程中食物影响研究技术指导原则》
[14] EMA.Guideline on the investigation of drug interactions.2012
[15] Cilla DD., et al. A Pilot Study Comparing Megestrol Acetate Concentrated Suspension (MA-CS) to Megestrol Acetate Oral Suspension (MA-OS) on Weight Gain and Body Composition in Patients with HIV-Associated Unintended Weight Loss (UWL)[J]. Blood 2005; 106 (11): 1433.
[16] Dobrila-Dintinjana R, Trivanovic D, Zelić M, Radić M,et al. Nutritional support in patients with colorectal cancer during chemotherapy: does it work? Hepatogastroenterology. 2013 May;60(123):475-80.
[17] Lin CY, Huang PW, Hsieh CH, Hsu CL, Liau CT, Huang SF, Liao CT, Chang TC, Wang HM. Prophylactic Versus Reactive Megestrol Acetate Use for Critical Body Weight Loss in Patients with Pharyngeal and Laryngeal Squamous Cell Carcinoma Undergoing Concurrent Chemoradiotherapy. Nutr Cancer. 2024;76(7):628-637.
[18] 醋酸甲地孕酮口服混悬液(美适亚®)说明书
[19] Rexrode KM, Manson J E. Are Some Types of Hormone Therapy Safer Than Others?: Lessons From the Estrogen and Thromboembolism Risk Study. Circulation 2007, 115(7): 820-822.
[20] Lee, C.M., Kang, J.H. & Go, SI. Clinical implication of megestrol acetate in metastatic gastric cancer: a big data analysis from Health Insurance Review and Assessment (HIRA) database.2024; Support Care Cancer 32, 249.
*来源于 健康时报,版权归原作者所有,如侵权请联系删除